바나듐레독스흐름전지의 전해질의 유량 변화에 따른 성능 영향성
2022 The Korean Hydrogen and New Energy Society. All rights reserved.
Abstract
In this study, the battery performance change according to the change of electrolyte flow rate. With increase of electrolyte flow rate the energy efficiency showed tendency of decrease. The electrochemical impedance spectroscopy results showed the increased resistance.
Keywords:
Vanadium redox flow battery, Vanadium, Electrolyte, Vanadium sulfide, Electrolyte flow rate키워드:
바나듐흐름전지, 바나듐, 전해질, 황산바나듐, 전해질유량1. 서 론
바나듐레독스흐름전지(vanadium redox flow battery, VRFB)는 외부 탱크에 저장된 수계 전해액이 배터리로 공급되어 충전과 방전을 하는 2차 배터리이다. VRFB는 양극과 음극의 전해액이 분리되어 외부 탱크에 저장되어 화재의 위험이 적고 수명이 리튬이온 배터리와 비교하였을 때 10배 이상 길다는 장점을 가지고 있다.
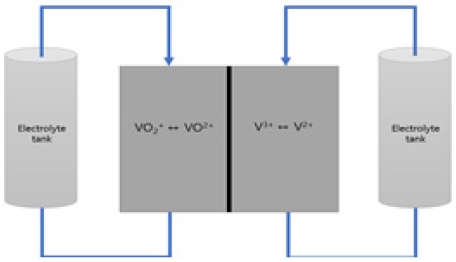
VRFB는 양극에서는 V4+와 V5+의 바나듐이 서로간의 산화/환원 반응이 이루어지고, 음극에서는 V3+와 V2+ 간의 산화/환원 반응이 이루어지면서 전력을 충/방전하는 장치이다. Fig. 1에서는 바나듐흐름전지의 모식도를 보여주고 있다. 그 화학식은 다음과 같다.
VRFB는 앞서 설명한 많은 장점이 있지만, 리튬이온 전지 대비 낮은 에너지 효율을 가지고 있고, 수계 전해액을 담기 위한 대용량의 탱크가 필요하기 때문에 소형화에 어려움이 있다. 이러한 문제점을 해결하기 위하여 많은 연구가 진행되고 있다. 대표적으로 VRFB용 탄소 전극에 다양한 개질을 통하여 낮은 에너지 밀도를 해결하기 위한 연구가 있다1-7).
Park과 Ko1)는 코발트 전구체를 grapihite felt 표면에 수열 처리법을 통하여 도입 후 열처리를 한 전극의 성능을 비교하였다. 개질한 전극이 다공성 표면과 Co의 촉매 효과로 다른 전극보다 우수한 전기화학적 성능을 보여주었다. Lim 등2)은 VRFB용 탄소전극에 산소와 질소의 도핑을 통하여 전기화학촉매의 특성 변화를 조사하였다. 전극 표면에 도핑되어진 산소와 질소 작용기들이 바나듐의 전기화학적 산화환원 반응을 촉진하는 것으로 나타났다. Hassan과 Tzedakis3)는 전기화학적 활성의 개선을 위해 화학적 개질 방법인 K2CrO7 산성 용액을 사용하였다. 그 결과 전기화학적 성질이 개선되어 효율과 내구성이 좋아졌다. Wang 등4)은 3D numerical model을 사용하여 채널의 형상이 각각 반원, 직사각형, 삼각형일 때의 이온의 이동과 바나듐흐름전지의 성능을 조사하였다. 반원 채널에서 전해액의 이동도가 개선되면서 가장 작은 과전위가 나타나 배터리의 성능이 개선되어졌다. Wang 등5)은 멤브레인 표면에 매우 작은 균열을 만들어 이온의 선택도를 개선시켰다. 그 결과 표면에 작은 균열을 가지고 있는 멤브레인이 일반적인 멤브레인보다 더 높은 에너지 효율을 보여주었다. Derr 등6)은 30일 동안 전해액에 담아 보관하여 전극의 산화가 배터리에 미치는 영향을 조사하였다. 반쪽 전지 테스트 결과 양극 반쪽 전지가 더 많은 산화를 보였지만 큰 성능 저하를 보이지 않고 음극의 산화에는 강한 영향을 받았다. Ha 등7)은 VRFB용 탄소 펠트의 산화 처리 방법이 전극 성능에 미치는 영향을 조사하였다. 500℃에서 열처리한 전극의 표면에 산소 관능기가 포함되고 산화 반응으로 인하여 생겨난 기공의 영향으로 반응면적이 넓어져 산화, 환원 특성이 우수하며 활성화 저항 또한 적게 나타났고, 과전압이 적게 나타났다. Oh 등8)은 VRFB용 전해액에 HSO3Cl을 첨가하여 제조하여 성능을 조사하였다. 그 결과 전해액의 활성이 높아져 에너지 효율이 높아진 것을 볼 수 있었다.
또한, 전극의 표면에 다른 물질을 첨가하는 방식의 연구도 진행되었다. Lee와 Kim9)은 VRFB용 탄소 전극에 산화그래핀을 이용하여 표면 처리를 하였다. 산화그래핀의 농도가 증가할수록 전기화학적 활성은 증가하지만 높은 농도에서는 오히려 반응면적이 줄어들어 활성이 줄어든 것으로 나타났다. 그리고 전극의 표면에 알칼리 처리와 기타의 물질을 이용한 개질 역시 진행되었다10,11). Jung 등10)은 VRFB용 탄소 전극에 KOH 용액을 침지시켜 전기화학적 산화를 유도하였다. 전해질 용액에 침지시킨 전극은 친수성 관능기의 도입으로 양극과 음극 쌍 사이의 가역성이 증가하였다. Choi와 Kim11)은 탄소 전극에 오존과 암모니아의 순차적 처리를 통하여 표면 처리를 하였다. 오존을 먼저 처리한 전극은 암모니아를 먼저 처리한 전극보다 표면에 더 많은 작용기가 생겨났다. 오존을 먼저 처리한 전극을 다른 샘플과 비교할 경우 더 높은 전기화학 활성과 방전용량이 더 높게 나타났다.
또한, VRFB의 충/방전 실험의 조건을 변화시켜 최적의 운전 조건을 찾기 위한 연구도 하였다12,13). Choi 등12)은 충/방전 실험 시 전류밀도의 크기를 증가시켜 성능을 비교하였다. 에너지 효율은 전류밀도 증가 시 감소하였으며 충/방전 실험 후 집전체에서의 부식 또는 벗겨짐 현상 및 전지의 온도 상승 현상은 관찰되지 않았다. Lee와 Kim13)은 전해질 유량과 전류 밀도의 변화를 주어 성능에 미치는 영향을 조사하였다. 그 결과 30 mL/min의 유량에서 가장 좋은 에너지 효율과 IR drop이 나타났다. 이는 유량이 과하게 증가하게 된다면 이온의 전극 표면 흡착이 어려워져 과전압이 높아지게 된다고 볼 수 있다. 본 논문에서는 외부의 탱크에서 배터리로 주입되는 전해액의 유량을 저, 중, 고로 변화시켜 이에 따른 VRFB의 성능 변화를 electrochemical impedance spectroscopy (EIS)와 충/방전 실험을 통하여 조사하였다7).
2. 실 험
2.1 VRFB용 전극 및 전해액의 제조
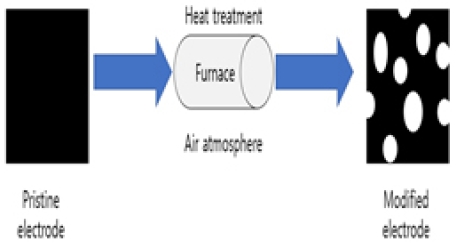
VRFB에 사용한 탄소 전극은 400℃에서 10시간 동안 고온로에서 공기 분위기로 열처리를 하였고, 전체적인 전극의 활성 면적은 4 cm2 (2×2 cm)로 제작하였다. 이 과정에서 카본펠트의 표면을 개질하여 카본펠트의 표면을 전극으로서 전기화학 반응이 가능하도록 만들어 본 실험을 실시하였다. 이 전체적인 과정은 Fig. 2에 나타내었다. 또한, 본 연구에 사용되는 전해액은 3 M의 황산 용액(H2SO4)을 지지전해질로 하여, 양극에는 1.6 M의 황산바나듐(VOSO4, V4+)을 저장하였고, 음극에서는 1.6 M의 V3+을 각각 외부에 마련된 탱크에 저장하였다.
2.2 바나듐흐름전지 단위셀의 운전 및 EIS
앞서 제작한 카본펠트 전극과 전해액을 사용한 단위전지를 이용하여 단위전지 운전을 실시하였다. Fig. 1은 단위전지 평가의 개념도를 나타낸다. 이 그림에서와 같이 양극과 음극에 각각의 전해질을 외부에 저장하여 펌프를 이용해 전해질을 순환시킨다. 전해질의 유량은 각각 1.6 mL/min, 2.4 mL/min, 3.75 mL/min로 설정하여 순환시켰고, 이를 각각 case 1, case 2, case 3으로 명명하였다. 이 때 양극과 음극의 전해질의 유량은 모두 같다. 그리고 충/방전 전류밀도는 모두 40 mV/cm2이고, 충전 과정에서 전압이 1.6 V에 도달하면 자동으로 방전을 시작하고, 방전과정에서 전압이 1.0 V에 도달하면 다시 충전모드로 전환되도록 설정하여 총 15사이클 동안 충/방전 실험을 수행하였다. 이 충/방전실험을 통하여 전류 효율(current efficiency, CE), 전압 효율(voltage efficiency, VE), 에너지 효율(energy efficiency, EE)을 구하였다.
마지막으로, 전기화학적 분석 방법인 EIS의 경우 정전류 모드에서 실시하였으며, 그 주파수 범위는 10 kHz부터 100 mHz까지 설정하였다.
3. 결과 및 고찰
Fig. 3은 배터리로 주입되는 전해액의 유량이 case 1 (Fig. 3[a]), case 2 (Fig. 3[b]), case 3 (Fig. 3[c])에서 시간의 변화에 따른 전압의 변화 그래프이다. 위의 그래프에서는 유량이 작아질수록 충전과 방전에 걸리는 시간이 짧아지는 것을 확인할 수 있다. 또한 유량이 증가할수록 I-R drop은 Fig. 3(a)에서 0.06727, Fig. 3(b)에서 0.04853, Fig. 3(c)에서는 0.12953이다.
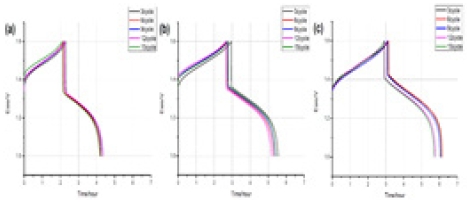
Results of case 1 (a), case 2 (b), and case 3 (c) from charge/discharge curve at a current density 40 mA/cm2.
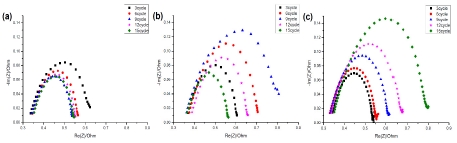
Fig. 4는 유량이 case 1 (Fig. 4[a]), case 2 (Fig. 4[b]), case 3 (Fig. 4[c])에서 저항의 크기를 EIS를 통해 분석하였다. 충/방전 사이클이 진행되는 동안 측정한 값을 표시하였다. Case 1에서는 사이클이 진행될수록 저항의 크기가 작아지다 9사이클 이후에는 큰 차이를 보이지 않는 것으로 나타났다. Case 2에서는 저항의 크기가 9사이클까지는 커지다가 그 이후부터는 저항의 크기가 작아져 15사이클의 저항은 3번째 사이클의 저항보다 더 작아졌다. Case 3에서는 사이클이 진행될수록 저항의 크기가 계속해서 커지고 있다.
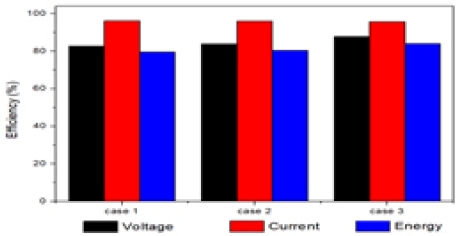
Fig. 5에서는 case 1, case 2, case 3에서의 전압 효율, 전류 효율, 에너지 효율을 나타냈다. 각 효율들의 값은 Table 1에 정리하였다. 전류 효율은 case 1에서 96.18%, case 2에서 95.92%, case 3에서 95.70%로 큰 차이를 보이지 않지만 전압 효율은 case 1에서 82.76%, case 2에서 83.82%, case 3에서 87.80%로 증가하였다. 에너지 효율은 case 1에서 76.59%, case 2에서 80.40%, case 3에서 84.02%로 유량이 증가할수록 더 높은 에너지 효율을 보여주었다.
4. 결 론
본 연구에서는 전해액 유량의 변화가 VRFB의 성능 변화를 충/방전실험과 EIS를 통하여 그 영향성을 조사하였다.
1) 전해액의 유량이 적을수록 충/방전 시간은 줄어드는 것을 볼 수 있었다.
2) 전기화학적 분석인 EIS 결과에서는 높은 유량에서 충/방전 사이클 횟수가 진행될수록 저항은 커지고, 유량이 적은 경우에는 저항이 작아졌다.
3) 충/방전실험 결과 높은 유량에서 전압 효율이 증가하면서 에너지 효율 역시 증가하는 것을 확인할 수 있었다.
4) 저유량에서는 EIS 분석 결과, 저항의 크기는 작아지고 충전과 방전에 걸리는 시간은 짧아지지만 상대적으로 에너지 효율이 적어짐을 확인할 수 있었다.
Acknowledgments
이 논문은 상지대학교 대학원의 지원을 받아 수행된 연구이다.
References
-
J. Park and M. Ko, “Improvement of cathode reaction of vanadium redox flow battery by reforming graphite felt electrode using cobalt oxide”, Journal of the Korean Institute of Surface Engineering, Vol. 52, No. 3, 2019, pp. 180-185.
[https://doi.org/10.5695/JKISE.2019.52.3.180]

-
H. Lim, J. Kim, J. S. Yi, and D. Lee, “Performance of carbon cathode and anode electrodes functionalized by N and O doping treatments for charge-discharge of vanadium redox flow battery”, Clean Technology, Vol. 23, No. 3, 2017, pp. 308-313.
[https://doi.org/10.7464/ksct.2017.23.3.308]

-
A. Hassan and T. Tzedakis, “Enhancement of the electrochemical activity of a commercial graphite felt for vanadium redox flow battery (VRFB), by chemical treatment with acidic solution of K2Cr2O7”, Journal of Energy Storage, Vol. 26, 2019, pp. 100967.
[https://doi.org/10.1016/j.est.2019.100967]

-
F. Wang, G. Xiao, and F. Chu, “Mass transfer enhancement in electrode and battery performance optimization of all-vanadium flow based on channel section reconstruction”, Chemical Engineering Journal, Vol. 451, No. P2, 2023, pp. 138619.
[https://doi.org/10.1016/j.cej.2022.138619]

-
T. Wang, S. J. Moon, D. S. Hwang, H. Park, J. Lee, S. Kim, Y. M. Lee, and S. Kim, “Selective ion transport for a vanadium redox flow battery (VRFB) in nano-crack regulated proton exchange membranes”, Journal of Membrane Science, Vol. 583, 2019, pp. 16-22.
[https://doi.org/10.1016/j.memsci.2019.04.017]

-
I. Derr, D. Przyrembel, J. Schweer, A. Fetyan, J. Langner, J. Melke, M. Weinelt, and C. Roth, “Electroless chemical aging of carbon felt electrodes for the all-vanadium redox flow battery (VRFB) investigated by Electrochemical Impedance and X-ray Photoelectron Spectroscopy”, Electrochimica Acta, Vol. 246, 2017, pp. 783-793.
[https://doi.org/10.1016/j.electacta.2017.06.050]

-
D. Y. Ha, S. K. Kim, D. H. Jung, S. Y. Lim, D. H. Peck, B. R. Lee, and K. Y. Lee, “Effect of carbon felt oxidation methods on the electrode performance of vanadium redox flow battery”, Journal of the Korean Electrochemical Society, Vol. 12, No. 3, 2009, pp. 263-270.
[https://doi.org/10.5229/JKES.2009.12.3.263]

-
Y. H. Oh, G. W. Lee, C. H. Ryu, and G. J. Hwang, “Study on the electrolyte added chlorosulfuric acid for all-vanadium redox flow battery”, Trans. of the Korean Hydrogen and New Energy Society, Vol. 27, No. 2, 2016, pp. 169-175.
[https://doi.org/10.7316/KHNES.2016.27.2.169]

-
K. J. Lee and S. Kim, “Electrochemical enhancement of carbon felt electrode for vanadium redox flow battery with grephene oxide”, Trans. of the Korean Hydrogen and New Energy Society, Vol. 28, No. 2, 2017, pp. 206-211.
[https://doi.org/10.7316/KHNES.2017.28.2.206]

-
Y. G. Jung, G. J. Hwang, J. C. Kim, and C. H. Ryu, “Electrochemical oxidation of carbon felt for redox flow battery”, Trans. of the Korean Hydrogen and New Energy Society, Vol. 22, No. 5, 2011, pp. 721-727.
[https://doi.org/10.7316/khnes.2011.22.5.721]

-
H. Choi and H. Kim, “Development of activated graphite felt electrode using ozone and ammonia consecutive post treatments for vanadium redox flow batteries”, Trans. of the Korean Hydrogen and New Energy Society, Vol. 32, No. 4, 2021, pp. 256-262.
[https://doi.org/10.7316/KHNES.2021.32.4.256]

-
H. S. Choi, D. M. In, Y. J. Song, C. H. Ryu, and G. J. Hwang, “Change of the efficiency in all-vanadium redox flow battery with current density”, Trans. of the Korean Hydrogen and New Energy Society, Vol. 28, No. 5, 2017, pp. 531-535.
[https://doi.org/10.7316/KHNES.2017.28.5.531]

-
K. J. Lee and S. H. Kim, “Effect of electrolyte flow rates on the performance of vanadium redox flow battery”, Trans. of the Korean Hydrogen and New Energy Society, Vol. 26, No. 4, 2015, pp. 324-330.
[https://doi.org/10.7316/KHNES.2015.26.4.324]