전기화학적 이산화탄소 포집 기술 개발
2024 The Korean Hydrogen and New Energy Society. All rights reserved.
Abstract
This study presents the development of an electrochemical carbon capture technology for direct air capture (DAC). The membrane-electrode assembly (MEA) design was optimized through the utilization of various commercial polymer electrolyte membranes and catalysts. Carbon capture ratio was evaluated using the fabricated MEA. As a result, we were able to demonstrate the feasibility of electrochemical carbon capture technology by showing a carbon capture ratio of approximately 87% in a simulated air gas containing 398 ppm of carbon dioxide.
Keywords:
Electrochemical cell, Carbon dioxide separation, Direct air capture, Carbon capture, Carbon dioxide removal키워드:
전기화학셀, 이산화탄소 분리, 직접 공기 포집, 탄소 포집, 이산화탄소 제거1. 서 론
산업화 이후 인간의 무분별한 화석연료 사용 등으로 인해 많은 양의 온실가스가 배출되었고 이로 인하여 지구 연평균 기온이 상승함에 따라 세계적으로 이상기후 현상 발생 빈도가 증가하고 있으며 특히 최근에는 지구 온난화(global warming) 시대를 넘어 지구 열대화(global boiling) 시대로 전환되었다고 유엔 사무총장이 언급한 바 있다. 따라서 이를 극복하기 위해 많은 국가들이 탄소 중립(carbon neutral)을 선언하고 온실가스 배출을 저감하기 위한 노력을 진행하고 있으며 우리나라 역시 2020년에 2050 탄소중립을 선언하고 net-zero를 달성하기 위한 다양한 노력을 수행하고 있다. 이러한 일환으로 정부에서는 ‘이산화탄소 포집·활용(carbon capture & utilization, CCU) 기술혁신 로드맵’을 발표하였고 ‘2050 탄소중립녹색성장위원회’ 출범 등의 노력을 기울이고 있으며 국내 연구자들도 이러한 탄소 포집 및 활용, 저장(carbon capture, utilization, & storage, CCUS) 기술 개발에 힘쓰고 있다1-4). 또한 2050년 net-zero를 달성하기 위하여 기후 변화에 관한 정부 간 협의체(Intergovernmental Panel on Climate Change, IPCC)에서는 「1.5℃ 특별보고서」를 발간하여 화석연료 사용 및 산업 부문에서의 탄소 배출량 저감과 더불어 이산화탄소 제거(carbon dioxide removal, CDR) 등의 완화 노력이 필요함을 언급하고 있다5,6). 이때 이러한 CDR 기술 중 하나로 대기 중의 이산화탄소를 제거할 수 있는 직접 공기 포집(direct air capture, DAC) 기술이 최근 크게 주목받고 있으나 저농도 이산화탄소를 포집해야 하는 이 기술의 경우 아직 기존 산업 현장에서 배가스 내의 고농도 이산화탄소를 포집하는 탄소 포집 기술 대비 연구 개발이 많이 진행되지 못하여 기술 수준이 낮은 실정이다7).
따라서 본 연구에서는 이러한 저농도의 이산화탄소를 포집하는 기술로써 전기화학적 방법을 활용하는 기술을 개발하고자 한다. 전기화학셀을 활용하여 이산화탄소를 포집하는 기술의 경우 기존 탄소 포집 방식 대비 국내외적으로 연구가 많이 이루어지진 않았지만 시스템의 크기를 간소화할 수 있다는 장점이 있어 해외에서도 관련 연구들이 점차 진행되고 있는 추세이다8-10). 다만 이러한 연구들은 아직 전기화학적으로 탄소를 포집하는 방법에 대한 실현 가능성 정도를 보는 데 그치고 있다. 본 연구에서는 전기화학적 탄소 포집 실현 가능성을 보다 높이고자 전기화학셀의 성능에 큰 영향을 끼치는 막-전극 접합체(membrane-electrode assembly, MEA)에 대한 설계 최적화를 수행하고자 한다. 전해질막 3종류와 anode 및 cathode 전극의 촉매 3종류에 대한 성능 평가 및 분석을 수행하고 이를 바탕으로 최적 설계한 MEA의 이산화탄소 포집률을 살펴보아 전기화학적 DAC 기술의 실현 가능성에 대해 알아보고자 한다.
2. 실험 장치 및 방법
2.1 MEA 제작
본 연구에서는 3종류의 상용 전해질막 및 3종류의 상용 촉매를 바탕으로 MEA를 제작하여 전기화학셀 성능을 분석하였다. 이때 전해질막은 FAA-3-50 (Fumatech, Bietigheim-Bissingen, Germany) 및 PiperION (Versogen, Newark, DE, USA), X37-50 (Dioxide Materials, Boca Raton, FL, USA)을 사용하였고 촉매는 Pt/C (60wt% Pt on Vulcan XC-72, Premetek, Cherry Hill, NJ, USA), Pt-Ir/C (40wt% Pt-Ir [1:1 atomic ratio] on Vulcan XC-72, Premetek), IrO2 99.99% (Alfa Aesar, Ward Hill, MA, USA) 등의 세 종류를 사용해 성능을 비교 분석하였다. 촉매와 ionomer (PiperION A5 ionomer; Versogen), DI-water, isopropyl alcohol를 이용하여 촉매 슬러리를 제조한 후 catalyst coated membrane (CCM) 방식으로 전해질막 위에 촉매 슬러리를 스프레이 방법으로 코팅하였으며 X37-50 전해질막의 경우 막의 특성상 건조 상태에서 부서지기 쉬워 catalyst coated substrate (CCS) 방식으로 gas diffusion layer (GDL) 위에 촉매를 코팅하였다. 이때 anode 혹은 cathode platinum group metals (PGM) 로딩량은 0.5 mg/cm2로 고정하였으며 IrO2의 경우 2 mg/cm2로 고정하였다. MEA의 활성화 면적은 5 cm2로 제작하였으며 이산화탄소 포집 성능 분석 시에는 25 cm2로 제작하여 실험을 수행하였다.
모든 MEA는 제작 후 실험 수행 전 전해질막 및 이오노머의 작용기를 CO32-로 치환하기 위해 1 M K2CO3 용액에 12시간 이상 전처리 후 DI-water로 rinsing하여 GDL (Sigracet 39BB, SGL Carbon, Wiesbaden, Germany) 과 함께 80 in·lb 토크로 unit cell (CNL Energy, Seoul, Korea) 조립을 수행하였다.
2.2 전기화학셀 MEA 성능 평가
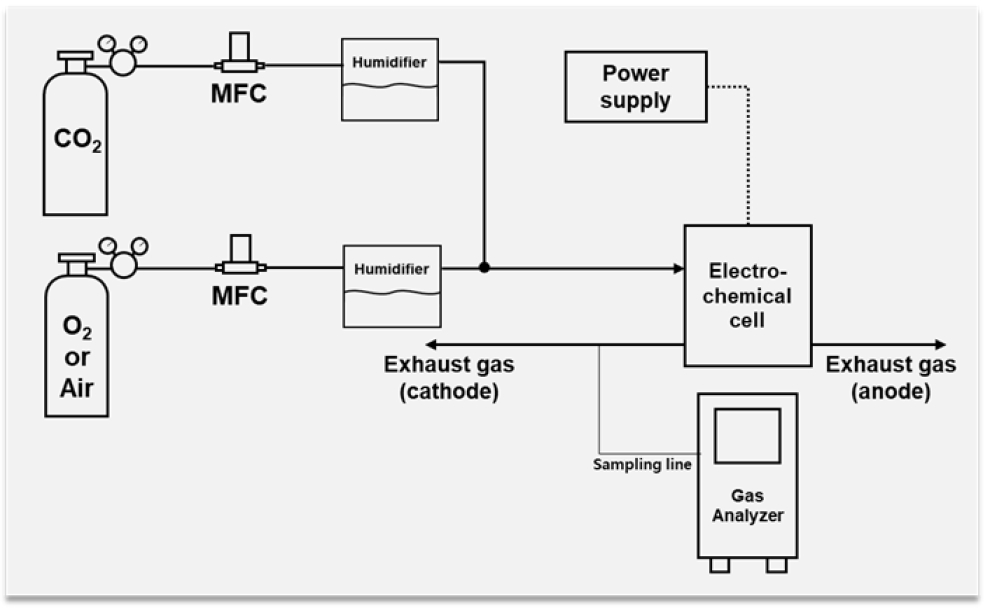
전기화학셀 성능 평가 장비(QSF, Seoul, Korea)를 활용하여 전기화학셀의 I-V 성능 측정을 수행하였으며 평가 장비 개략도는 Fig. 1과 같다. 전기화학셀에 공급하는 CO2 가스는 평가 장비 내 가스 유량 제어기(F-201CL-025; Bronkhorst High-Tech BV, Ruurlo, Netherlands)를 이용해 유량을 조절하여 공급하였으며 O2의 경우 가스 유량 제어기(F-201CL-013; Bronkhorst High-Tech BV)를 이용해 유량을 조절하여 공급하였다. 공급되는 가스는 모두 버블러 타입의 가습 장치를 통해 전기화학셀에 공급되며 이때 dew point 조절을 통해 가스의 가습량을 조절하였다. CO2 및 O2 가스는 mixing 후 전기화학셀의 cathode 측에 공급되며 anode 측으로는 별도의 가스를 공급하지 않았다. 모든 실험은 작동온도 60℃에서 수행하였으며 CO2 및 O2 유량은 1,000 sccm 및 250 sccm이고 상대습도 100% 기준으로 공급하였다. 전기화학셀에 직류 전원 공급 장치(PWR801L; Kikusui, Yokohama, Japan)를 사용해 전원을 공급하였으며 이때 I-V 성능 측정을 위해 0.1 V부터 1.2 V까지 0.05 V 간격으로 데이터 획득을 수행하였다.
2.3 이산화탄소 포집 성능 평가
본 연구에서는 대기 중의 이산화탄소를 포집하는 기술인 DAC 기술을 전기화학셀을 활용하여 구현할 수 있는지 알아보기 위해 대기 조성을 모사한 20.8%의 O2 및 398 ppm CO2를 포함하는 N2 base 합성 가스를 제작하여 합성 가스 내의 CO2 포집률에 대해 알아보고자 하였다. 이와 더불어 실내 등 환경에서 이산화탄소가 농축된 환경도 모사하기 위하여 1,000 ppm 및 2,000 ppm의 이산화탄소를 포함하는 공기 모사 가스 역시 제작하였고 제작한 합성 가스를 전기화학셀 cathode 측으로 유량을 제어하며 공급하였다. 전기화학셀 cathode 측 exhaust gas line에서 sampling line을 분기하여 gas analyzer (URAS26; ABB, Zurich, Switzerland)를 활용해 CO2 농도를 측정할 수 있게끔 하였다. 이때 non-dispersive infrared (NDIR) 분광법을 통해 0-3,000 ppm 및 0-25 vol% 농도 측정이 가능하게 하였다.
이산화탄소 포집률의 경우 대기 중의 이산화탄소 양이 매우 작기 때문에 전기화학셀 cathode 측의 입출구 유량의 변화가 크지 않다고 가정하여 식 (1)과 같이 포집률 계산을 수행하였다.
| (1) |
3. 결과 및 고찰
3.1 전해질막 종류에 따른 MEA 성능 분석
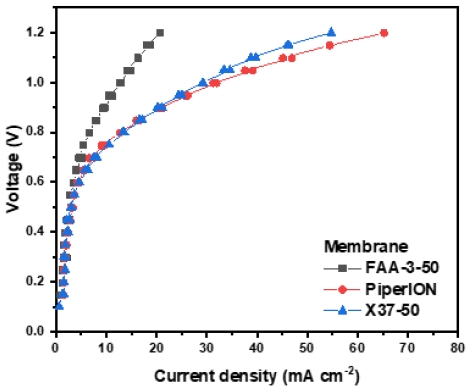
전기화학적 이산화탄소를 분리 및 포집하는 기술의 실현 가능성을 알아보기 위하여 본 연구에서는 앞서 언급하였듯이 FAA-3-50 및 PiperION, X37-50 등 총 세 종류의 상용 전해질막을 활용하여 MEA를 제작해 성능 분석을 수행하였다. MEA를 제작할 때 anode 및 cathode 측 촉매는 모두 Pt/C 촉매를 사용하여 0.5 mg/cm2씩 로딩하였다.
그 결과 Fig. 2의 polarization curve에서 볼 수 있듯이 PiperION이 1.2 V에서 가장 높은 전류밀도를 보여주는 것을 확인할 수 있었다. 이는 PiperION 전해질막의 이온전도도가 타 전해질막 대비 높기 때문임을 유추할 수 있었으며11) 동일 전압에서 가장 높은 전류밀도를 보여준 PiperION 전해질막이 전해질막을 통해 전달되는 이온의 양이 가장 많기 때문에 이산화탄소 포집률 또한 높을 것으로 추론할 수 있다. 따라서 탄소 포집을 위한 MEA 제작에 있어서 전해질막은 최종적으로 PiperION으로 선정하였다.
3.2 촉매 종류에 따른 MEA 성능 분석
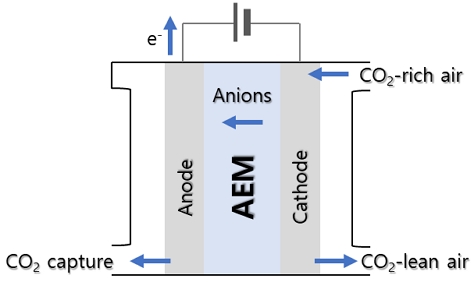
전기화학셀을 활용해 CO2를 분리하는 작동 원리는 Fig. 3 및 식 (2)-(9)와 같다. 전기화학셀 cathode 측에 가습된 O2 및 CO2를 공급하면 식 (2)-(4) 및 (8), (9)와 같이 전기화학 반응 및 산-염기 반응에 의하여 (중)탄산 이온이 생성되고 이는 전해질막을 통해 anode 측으로 넘어간다. Anode 측에 넘어온 (중)탄산 이온은 식 (5)-(9)와 같이 cathode에서의 역반응이 일어나 다시 O2 및 CO2를 발생시킨다. 즉 O2를 carrier gas로 하여 CO2가 cathode 측 공급 가스 내에서 anode 측으로 분리된다.
| (2) |
| (3) |
| (4) |
| (5) |
| (6) |
| (7) |
| (8) |
| (9) |
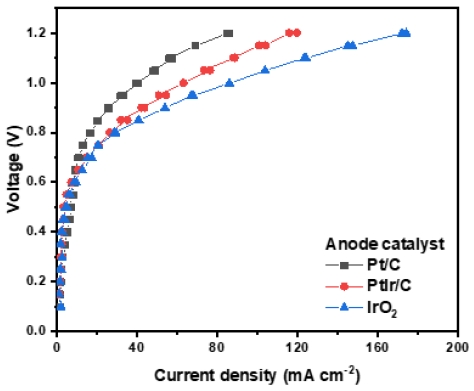
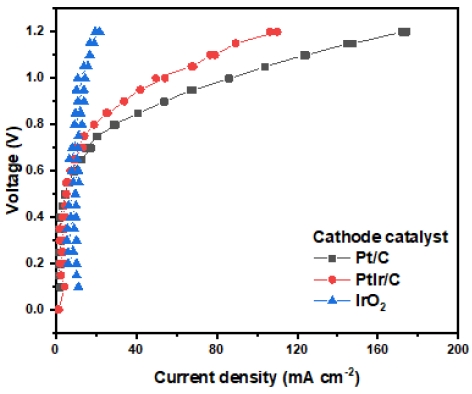
이때 이러한 전기화학 반응은 사용하는 촉매에 따라 각기 다른 반응 속도를 보이고 이러한 반응 속도를 높이기 위해 본 연구에서는 2.1절에서 언급한 Pt/C, Pt-Ir/C, IrO2 등 3종류 촉매를 사용하여 제작한 MEA의 성능에 대해 살펴보았다. 이때 anode 및 cathode 측에 각각 적합한 촉매를 선정하기 위해 우선 anode 측에 세 종류의 촉매를 활용하여 성능 분석을 수행하였고 이때 cathode 측 촉매는 Pt/C 촉매로 고정하였다.
그 결과 Fig. 4의 polarization curve에서 볼 수 있듯이 anode 측 촉매의 경우 IrO2 촉매가 1.2 V에서 가장 높은 전류밀도를 보여주는 것을 확인할 수 있었다. 이는 앞선 전기화학 반응식에서처럼 cathode에서 anode로 (중)탄산 이온이 이동하여 anode에서 CO2 및 O2가 발생하게 되는데 이때 O2의 경우 촉매 표면에서 O2를 포함하는 중간 매개체들과 4전자와의 heterogeneous 반응으로 생성되므로 금속 산화물 촉매에서 더 우수한 활성을 보이기 때문으로 사료된다.
Cathode 측에 적합한 촉매 역시 선정할 필요가 있으며 이를 위해 anode 측에서 가장 높은 성능을 보인 IrO2 촉매를 anode 촉매로 고정하고 이후 cathode 촉매의 경우 앞선 세 종류의 촉매를 적용하여 성능 분석을 수행하였다.
그 결과 Fig. 5의 polarization curve에서 볼 수 있듯이 Pt/C 촉매가 1.2 V의 높은 전압 구간에서 가장 높은 성능을 보여주는 것을 확인할 수 있었으며 특히 금속 산화물 촉매 대비 Pt 계열의 촉매에서 월등한 성능을 보이는 것을 알 수 있었다. 이는 앞선 cathode에서의 전기화학 반응식에서 (중)탄산 이온이 생성되는 반응의 경우 우선적으로 산소 환원 반응이 일어난 후 (중)탄산 이온이 생성되는데 이때 산소 환원 반응의 경우 Pt 계열의 촉매가 더 적합한 촉매이기 때문에 금속 산화물 촉매 대비 월등한 성능을 보인 것으로 사료된다. 특히 Pt/C 촉매가 PtIr/C 촉매 대비 더 높은 성능을 보이는데 이 역시 Pt 합금 촉매보다 Pt 촉매가 산소 환원 반응에 더 적합하기 때문이다.
3.3 이산화탄소 포집 성능 분석
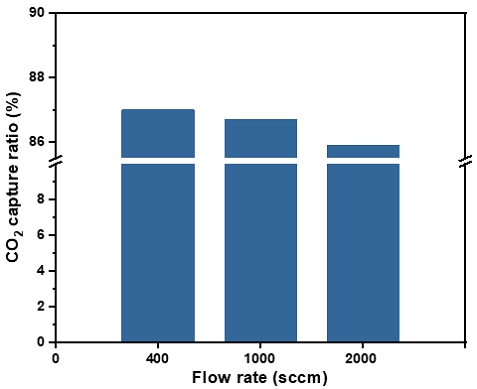
앞서 전해질막 및 촉매 종류에 따른 MEA 성능 분석을 수행한 후 가장 높은 성능을 보였던 PiperION 전해질막과 anode 촉매로 IrO2, cathode 촉매로 Pt/C를 사용하여 25 cm2의 MEA를 제작하여 이산화탄소 포집 성능 분석을 수행하였다. 이때 2.3절에서 언급한 바와 같이 약 400, 1,000, 2,000 ppm의 이산화탄소를 포함하고 있는 공기 모사 가스를 활용하여 유량 제어기를 통해 500 sccm의 유량으로 전기화학셀에 가스를 공급하여 셀에서 토출된 가스 내 이산화탄소 농도를 바탕으로 셀의 이산화탄소 포집률을 계산하였다.
그 결과 Fig. 6과 같이 대기 중의 이산화탄소 농도와 비슷한 약 400 ppm의 이산화탄소를 포함하는 공기 모사 가스를 셀에 공급하였을 때 약 87% 수준의 이산화탄소 포집률을 보였다. 이산화탄소가 농축된 실내 환경을 모사한 약 1,000, 2,000 ppm의 이산화탄소를 포함하는 공기 모사 가스의 경우 각각 이산화탄소 포집률 86.7% 및 85.9%를 보여주었다. 세 가지 조건 모두 85% 이상의 탄소 포집률을 보여주어 공기 중 이산화탄소를 포집하는 DAC 기술로의 전기화학셀 활용 가능성에 대해서 충분히 입증할 수 있었다. 추후 연구에서는 전극 조성 및 두께 등 MEA에 대한 최적화와 더불어 분리판 및 셀 작동 조건에 대한 최적화를 수행한다면 전기화학셀에서의 탄소 포집률을 더욱 높일 수 있을 것으로 기대한다.
4. 결 론
본 연구에서는 음이온 교환막을 활용한 전기화학적 방법으로 이산화탄소를 대기 중에서 분리 및 포집하는 기술의 실현 가능성에 대해 살펴보았다. 총 세 종류의 상용 음이온 교환막과 세 종류의 촉매를 각각 anode 및 cathode에 사용하여 가장 높은 성능을 보이는 MEA 조합을 찾았으며 결과는 다음과 같다.
1) 본 연구에서는 총 세 가지 종류의 상용 음이온 교환막을 활용하여 제작한 MEA의 성능 분석을 수행하였고 1.2 V 조건에서 PiperION 전해질막이 가장 높은 성능을 보여주었다.
2) Anode 및 cathode 촉매로 각각 세 종류의 촉매에 대한 성능 분석을 수행하였고 그 결과 anode 촉매는 산소 발생 반응에 적합한 IrO2 촉매, cathode 촉매는 산소 환원 반응에 적합한 Pt/C 촉매가 가장 우수한 성능을 보여주었다.
3) 가장 높은 성능을 보여준 전해질막과 촉매들을 바탕으로 MEA를 제작하였고 이를 바탕으로 약 400, 1,000, 2,000 ppm 등 세 가지 농도의 이산화탄소를 포함하는 공기 모사 가스로 이산화탄소 포집률에 대한 분석을 수행하였다. 그 결과 각각 약 87.0, 86.7, 85.9% 수준의 탄소 포집률을 보여주어 DAC 기술의 실현 가능성에 대해 충분히 입증할 수 있었다.
Acknowledgments
본 연구는 한국기계연구원 기본사업(창의·도전형 과제) “전기화학셀을 활용한 CO2 분리/압축 기술 개발(NK245H)” 및 한국기계연구원 기본사업 “차세대 암모니아 연료전지 스택 및 시스템 개발(NK249F)”의 지원으로 수행되었습니다.
References
- J. H. Choi, J. T. Jang, S. H. Yun, W. H. Jo, J. Y. Jung, and Y. I. Yoon, “Effect on the heat of reaction to temperature and absorption capacity in the reaction of cyclic amines with carbon dioxide”, Journal of Hydrogen and New Energy, Vol. 29, No. 5, 2018, pp. 530-537.
-
J. Choi, Y. Yoon, S. Park, I. Baek, Y. Kim, and S. Nam, “Thermal degradation of aqueous MEA solution for CO2 absorption by nuclear magnetics resonance”, Journal of Hydrogen and New Energy, Vol. 27, No. 5, 2016, pp. 562-570.
[https://doi.org/10.7316/KHNES.2016.27.5.562]

- S. Y. In, Y. J. Lee, S. C. Lee, and J. C. Kim, “CO₂ capture technology and market trends to realize carbon neutrality”, Journal of Energy & Climate Change, Vol. 19, No. 1, 2024, pp. 132-144.
-
S. Heo, W. Kim, and Y. M. Jo, “Preparation and characterization of bamboo-based activated carbon for low-level CO2 adsorption”, Journal of Korean Society for Atmospheric Environment, Vol. 40, No. 1, 2023, pp. 48-58.
[https://doi.org/10.5572/KOSAE.2024.40.1.48]

- Intergovernmental Panel on Climate Change (IPCC), “Global warming of 1.5℃”, IPCC, 2018, pp. 616. Retrieved from https://www.ipcc.ch/sr15/, .
-
Intergovernmental Panel on Climate Change (IPCC), “Climate change 2022: mitigation of climate change”, IPCC, 2022. Retrieved from https://www.ipcc.ch/report/ar6/wg3/, .
[https://doi.org/10.1017/9781009157926]

-
Y. Song and C. Oh, “Korea’s policy direction on the research & development of direct air carbon capture and storage (DACCS) technologies: focusing on DAC technologies”, Journal of Climate Change Research, Vol. 13, No. 1, 2022, pp. 75-96.
[https://doi.org/10.15531/KSCCR.2022.13.1.075]

-
S. Matz, L. Shi, Y. Zhao, S. Gottesfeld, B. P. Setzler, and Y. Yan, “Hydrogen-powered electrochemically-driven CO2 removal from air containing 400 to 5000 ppm CO2”, Journal of The Electrochemical Society, Vol. 169, No. 7, 2022, pp. 073503.
[https://doi.org/10.1149/1945-7111/ac7adf]

-
S. Matz, B. P. Setzler, C. M. Weiss, L. Shi, S. Gottesfeld, and Y. Yan, “Demonstration of electrochemically-driven CO2 separation using hydroxide exchange membranes”, Journal of The Electrochemical Society, Vol. 168, No. 1, 2021, pp. 014501.
[https://doi.org/10.1149/1945-7111/abd5fe]

-
A. P. Muroyama, A. Beard, B. Pribyl-Kranewitter, and L. Gubler, “Separation of CO2 from dilute gas streams using a membrane electrochemical cell”, ACS ES&T Engineering, Vol. 1, No. 5, 2021, pp. 905-916.
[https://doi.org/10.1021/acsestengg.1c00048]

-
J. E. Chae, J. Choi, S. Lee, C. Park, and S. Kim, “Effects of fabrication parameters of membrane–electrode assembly for high-performance anion exchange membrane fuel cells”, Journal of Industrial and Engineering Chemistry, Vol. 133, 2024, pp. 255-262.
[https://doi.org/10.1016/j.jiec.2023.11.063]