메탄의 열적 분해에 따른 전환율 및 수소 생성에 관한 수치해석 검증 및 예측에 관한 연구
2025 The Korean Hydrogen and New Energy Society. All rights reserved.
Abstract
Hydrogen is one of the most promising energy sources that reduce carbon dioxide emissions from fossil fuel-based energy systems. In this study, numerical simulation was conducted to predict the chemical behaviors of methane conversion into hydrogen according to parameters such as temperature, CH4 flow rate, and pressure. The chemical mechanism for methane decomposition was validated with the experiments. As the temperature increased and the CH4 flow rate decreased, the methane conversion rate increased and the hydrogen yield can be obtained more than 70% since the reaction rate and residence time were increased. Although high pressure inhibited methane decomposition, pressure can be considered as a selective parameter for hydrogen yield.
Keywords:
Methane decomposition, Hydrogen production, Methane conversion rate, Mechanism validation, Parametric evaluation키워드:
메탄 분해, 수소 생산, 메탄 전환율, 반응 기구 검증, 매개변수 평가1. 서 론
현재 온실가스 배출 및 지구온난화에 따른 기후 변화에 대한 인식이 증가함에 따라 전 세계적으로 탄소 중립 전략에 대한 가속화가 진행되고 있다. 특히 신재생에너지, 바이오에너지와 무탄소계 연료로의 전환은 온실가스 배출에 의해 발생하는 지구온난화를 해결하는 데 중요한 역할을 한다. 그중 수소는 무탄소계 에너지원으로 기존의 온실가스 다배출 산업에서는 탄화수소에서 수소로의 전환을 통해 이산화탄소 저감을 기대할 수 있다. 하지만 기존의 수소 생산 공정만으로는 수소의 대량 생산을 충족하는 것이 어렵기 때문에 경제적이고 실용적인 기술이 필요하다.
수소 생산 기술 중 메탄 열분해에 대한 관심이 높아지고 있다. 메탄 열분해는 메탄의 열화학적 전환을 통해 수소를 생산하며 식 (1)과 같이 이론적으로 메탄이 수소와 고체 탄소로 분해될 때 이산화탄소가 발생하지 않는다. 이상적인 조건에서 1몰의 수소를 생산하기 위하여 필요한 최소 에너지 요구량은 37.8 kJ/mol로 수증기 메탄 개질 반응의 41.25 kJ/mol 대비 상대적으로 적은 에너지를 필요로 한다1). 이외에도 기존 천연가스 인프라를 활용할 수 있으며 메탄 열분해의 부산물인 탄소는 다양한 산업군에서 원료 혹은 제품으로 활용 가능하다.
| (1) |
무촉매 조건에서의 메탄 열분해는 1,000℃ 이상의 고온을 필요로 한다. 기존의 촉매 활용 메탄 열분해의 경우 낮은 온도(<800℃)에서 C-H 결합 분해를 촉진시키기 위하여 Co, Ru, Ni, Rh 등 고체 촉매가 주로 사용되었으나2) 부산물인 고체 탄소가 촉매 표면에 축적되는 코킹(coking) 현상으로 인해 촉매의 활성도가 저하된다3). 이러한 고체 촉매의 비활성화를 방지하기 위하여 용융 금속 촉매가 주목받고 있다. Hu 등4)은 Ni-Fe/Al2O3 촉매를 활용하여 800℃에서의 메탄 촉매 분해의 안정성 및 탄소 생성 특성을 확인하고자 하였다. 용융염이 활성화된 Ni-Fe/Al2O3 촉매는 1,000분 동안 높은 활성도를 보였으며 메탄 전환율 81%를 달성하여 메탄 촉매 분해의 장기적인 안정성을 나타내었다. 용융염이 있는 촉매를 사용하였을 때 촉매 상단에 탄소 나노 필라멘트가 대량으로 포집되었으며 용융염이 없는 촉매의 경우 작은 입자 형태의 탄소가 생성되었다.
Mokashi 등5)은 메탄 열분해 실험 결과를 기반으로 1차원 plug flow reactor (PFR) 모델을 활용하여 메탄 열분해 반응을 모사하였다. 그리고 온도, 반응물 조성, 체류 시간 등 매개변수에 따른 수소 및 고체 탄소 생성을 분석하고자 수치해석 연구를 수행하였다. 실험 결과 1,000℃ 이상 온도에서 메탄 전환이 시작되며 1,300℃까지 온도가 상승함에 따라 최대 메탄 전환율 및 최대 수소 수율의 결과를 나타냈다. 반응물인 CH4-H2 혼합 가스에서 H2 비율이 높을수록 메탄 전환율은 감소하고 그을음 생성이 억제되는 것을 예측하였다. 이에 따라 공급 가스에 수소를 추가하는 것은 부산물 형성을 제어하는 데 중요한 매개변수임을 밝혔다.
Carretta 등6)은 탄소 침적이 반응기 내 반응 효율을 저하시키고 반응기를 막는 문제를 해결하기 위하여 computational fluid dynamics (CFD) 수치해석 연구를 통한 탄소 침적 과정을 예측하고자 하였다. 빈 반응기의 경우 반응 온도 1,100℃에서 메탄 전환율이 50% 이상이나 15일 만에 반응기가 막히는 것으로 예측되었다. 충전층 반응기는 반응 표면적의 증가로 초기 반응 효율을 증가시키나 긴 체류 시간 조건에서 공극률이 감소함에 따라 성능이 저하되는 결과를 도출하였다.
Khrabry 등7)은 carbon black, graphite 등 탄소 생성 공정을 개선하기 위하여 나노 구조를 가진 탄소 및 그을음 형성을 예측하고자 화학 메커니즘 개발 및 성능 평가를 수행하였다. 기존의 ABF2000 및 Tao 화학 반응 기구를 기반으로 C2H2, 다환 방향족 탄화수소(polycyclic aromatic hydrocarbon, PAH) 및 hydrogen abstraction carbon addition (HACA) 경로를 포함한 최대 37개의 방향족에 대한 화학 반응을 고려하였으며 다양한 온도, 체류 시간, 메탄 희석 조건에서 실험 결과와의 비교를 통해 메커니즘의 유효성을 검증하였다. PAH 분자는 carbon nanotube 합성의 전구체로 작용하여 C2H2의 소비율 및 PAH 생성의 예측 정확성을 높이고자 하였다. 1,400℃에서 메탄 열분해 반응에 의하여 C2H2 농도가 감소함에 따라 PAH 생성량이 증가하였으며 반응물 내 CH4 농도가 높을수록 PAH 생성에 유리한 것으로 예측되었다.
Chen 등8)은 천연가스를 원료로 한 2단계 연소 열분해 반응기를 활용하여 매개변수에 따른 아세틸렌 생산 특성을 분석하고 GRI-Mech 3.0을 적용한 Cantera 1차원 수치해석을 통해 C2+ 및 합성 가스(syngas) 형성 반응 경로를 분석하였다. 2단계 연소 열분해를 통해 85.1%의 메탄 전환율 및 20.4%의 C2+ 수율 특성을 보였으며 수치해석을 통해 혼합 시간이 C2+ 수율 제어에 중요한 매개변수임을 보고하였다. Fau 등9)은 선행 연구를 통해 보고된 다양한 화학 반응 기구를 조사하고 화학 반응 기구에 대한 검증을 위하여 실험 결과10,11)에 따른 메탄, 수소 및 아세틸렌에 대한 불일치율을 분석하였다. Hamdullahpur에 의해 제안된 화학 반응 기구는 체류 시간과 온도에 따라 기존 화학 반응 기구의 수소 생산량에 대한 불일치율을 최대 15% 정도 감소시켰다.
따라서 본 연구의 목적은 수치해석과 실험과의 비교를 통해 메탄 열분해 모사를 위한 화학 반응 기구를 검증하고 검증된 화학 반응 기구를 활용하여 1차원 PFR 모델에서의 온도, 압력, 유량 등 매개변수에 따른 메탄 분해, 수소 및 탄화수소 생성 등의 화학적 거동을 예측하고자 한다. 이를 통해 메탄의 열적 분해에 따른 수소 생성 거동에 대한 매개변수의 민감도를 조사하고 수소 수율 증대를 위한 주요 매개변수를 평가하고자 한다.
2. 수치해석 방법 및 조건
본 연구에서는 메탄 열분해 모사를 위한 화학 반응 기구의 검증을 위하여 Jang 등12)에 의해 수행된 실험 조건에 대한 수치해석을 수행하였으며 해석 모델로는 0차원 perfectly stirred reactor (PSR)를 적용하였다. 선행 연구를 살펴보면 Jang 등12)은 상압 조건에서 메탄을 250 mL/min 투입하였으며 반응 온도는 약 1,052-1,302℃의 고온 조건에서 실험을 수행하였다. 본 연구의 검증을 위해 활용된 화학 반응 기구로는 Hamdullahpur13), Aramco14), GRI-Mech 3.015), Konnov16) 및 Westbrook17)이 있으며 선행 연구를 통해 제안된 화학 반응 기구를 기반으로 실험과의 비교를 통해 검증을 수행하였다. 화학 반응 기구의 검증은 식 (2)와 같이 정의된 오차율에 의해 평가되었다.
| (2) |
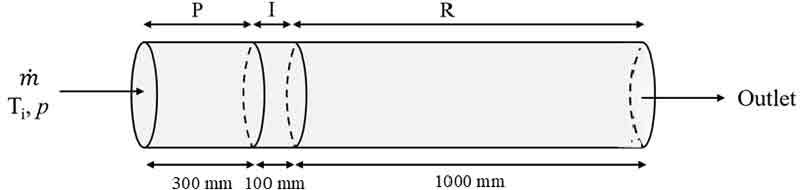
본 연구에서는 메탄의 열적 분해에 따른 화학적 거동 분석과 매개변수에 따른 특성 평가를 위하여 1차원 PFR 모델을 활용하였다. 수치해석에 적용된 반응기 형상은 Fig. 1의 직경 28 mm, 길이 1,400 mm의 실린더형 반응기를 가정하였으며 예열, 단열 그리고 열분해 영역으로 구분하였다. Table 1에 제시된 바와 같이 무촉매 조건에서 메탄 열분해에 대한 특성 분석을 위한 매개변수로 반응 온도는 주 반응 영역을 기준으로 1,000-2,000℃를 적용하였으며 반응 압력은 1-30 atm을 고려하였다. 메탄 투입 유량은 0.1-2.0 g/min으로 설정하였다. 모든 반응기 입구에서의 온도는 상온을 가정하였으며 메탄 예열 온도는 800℃로 고정하였다.
메탄 열분해의 특성은 메탄 전환율 및 수소 수율을 통해 특성화하였으며 식 (3) 및 (4)와 같이 정의하였다18).
| (3) |
| (4) |
여기서 CH4,inlet은 반응 전 메탄 유량, CH4,outlet은 반응 후 잔류 메탄 유량을 의미한다. 메탄 전환율은 열분해를 통해 투입된 메탄이 다른 생성물로 전환된 정도이고 수소 수율은 메탄 열분해 반응으로부터 이론적으로 생성될 수 있는 수소 질량 대비 실제로 생성된 수소 질량에 대한 정도를 의미하며 식 (1)을 통해 계산할 수 있다.
3. 결과 및 고찰
3.1 메탄 열분해 화학 반응 기구의 검증
메탄의 열화학적 전환 모사를 위한 화학 반응 기구에 관한 연구는 오랫동안 지속되고 있으며 특히 메탄은 다양한 수치해석 연구에서 천연가스의 모사 연료(surrogate fuel)로 적용되고 있다. 본 연구에서는 메탄 열분해 반응 모사를 위한 화학 반응 기구를 선정하고자 하였다.
Fig. 2는 메탄 전환율 및 수소 몰 분율에 대해 실험과 해석 결과를 화학 반응 기구별로 비교한 결과이다. Fig. 2에서 실험 결과와 비교하였을 때 메탄 전환율과 수소 몰 분율에서 정성적으로 모든 화학 반응 기구가 실험과 유사한 경향을 예측하였다. 그중 Hamdullahpur가 제안한 화학 반응 기구는 메탄 전환율 및 수소 몰 분율 모두 실험과 정량적으로 유사한 예측 결과를 보였다. Fig. 2(a)의 메탄 전환율을 보면 Aramco와 Konnov가 제안한 화학 반응 기구는 서로 동일한 수준의 예측 결과를 보였다. 하지만 Fig. 2(b)인 수소 몰 분율에서 Hamdullahpur가 제안한 화학 반응 기구를 제외한 나머지 화학 반응 기구의 경우 반응 온도가 증가함에 따라 실험 결과와의 차이가 증가하는 것으로 예측되었다.
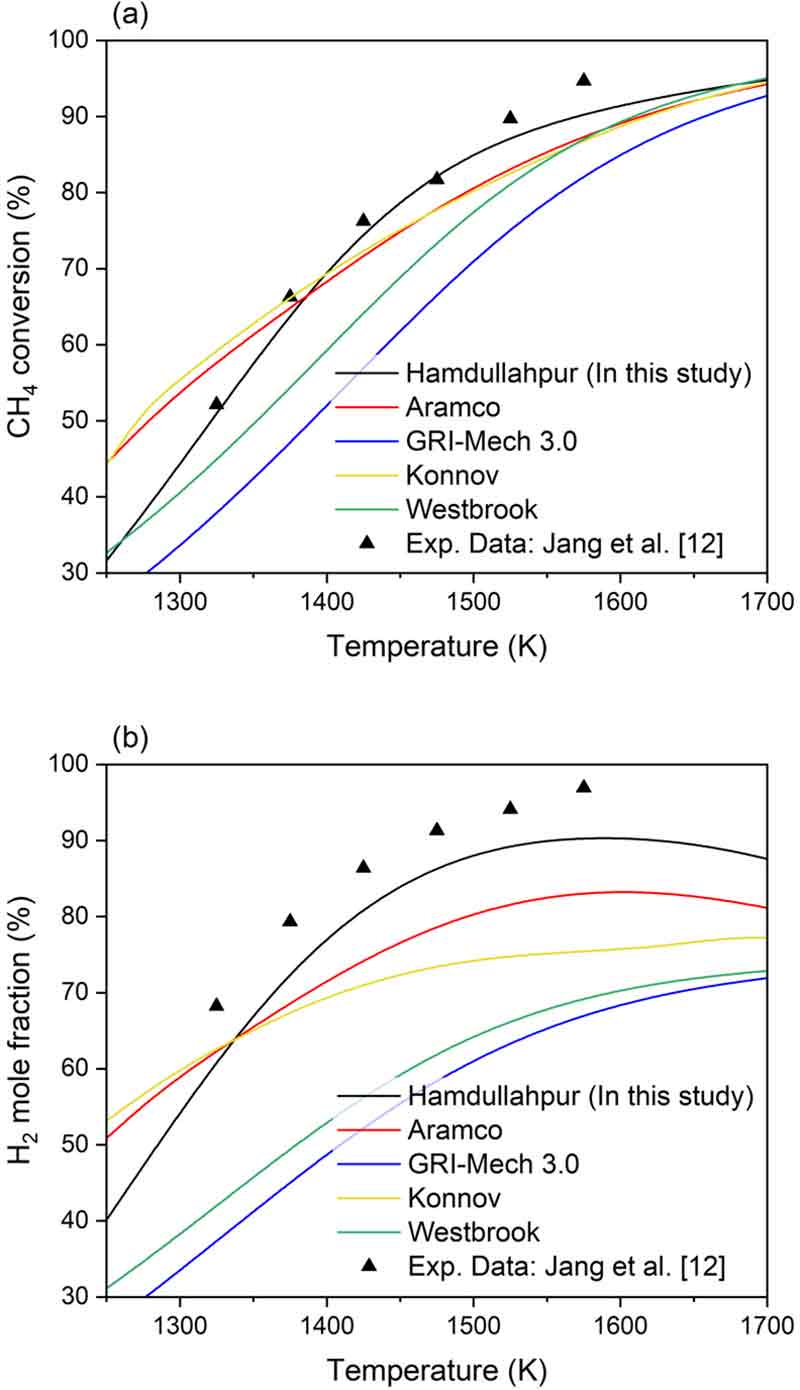
Validation and comparison of experimental data and reaction mechanisms by PSR model. (a) CH4 conversion. (b) H2 mole fraction
Fig. 2에서 예측된 결과에 대한 정량적 분석을 위하여 식 (2)를 활용하여 평균 오차율을 도출하였으며 결과는 Table 2와 같다. Hamdullahpur에 의해 제안된 화학 반응 기구는 메탄 전환율과 수소 몰 분율 모두 10% 이내의 오차율을 보였다. 이외 화학 반응 기구의 경우 전반적으로 메탄 전환율에 대한 오차는 20% 내외 수준으로 비교적 높은 예측성을 보였으나 수소 몰 분율의 경우 Aramco와 Konnov에 의해 제안된 반응 기구를 제외하고 모두 30% 이상의 오차를 보였다. 따라서 메탄 열분해의 화학 반응 모사를 위해서는 Hamdullahpur, Aramco, Konnov에 의해 제안된 화학 반응 기구가 적절한 것으로 평가되었으며 본 연구에서는 메탄 전환율 및 수소 몰 분율에 대해 가장 높은 정확도를 보인 Hamdullahpur에 의해 제안된 화학 반응 기구를 활용하여 메탄 열분해 매개변수에 대한 민감도를 조사하고 메탄 전환 및 수소 생성에 대한 예측 및 분석을 수행하였다.
3.2 메탄 열분해 매개변수별 민감도 조사 및 분석
본 연구에서는 3.1절에서 검증된 화학 반응 기구를 활용하여 Table 1에 제시된 조건을 기준으로 Fig. 1의 PFR 모델에서의 매개변수별 메탄 열분해 특성에 대한 민감도 조사와 예측 연구를 수행하였다. Fig. 3은 온도 및 압력에 따른 메탄 유량별 반응기 출구에서의 메탄 및 수소의 질량 분율과 메탄 전환율을 예측한 결과이다. Fig. 3(a)에 도시된 바와 같이 모든 조건에서 온도가 증가함에 따라 메탄의 열화학적 전환으로 인해 생성된 수소 질량 분율은 증가할 것으로 예측되었으며, 이는 자명하다. 특히 온도가 높을수록, 메탄 유량이 낮을수록 메탄의 질량 분율이 크게 감소하였으며 수소의 질량 분율은 증가하는 것을 알 수 있다.
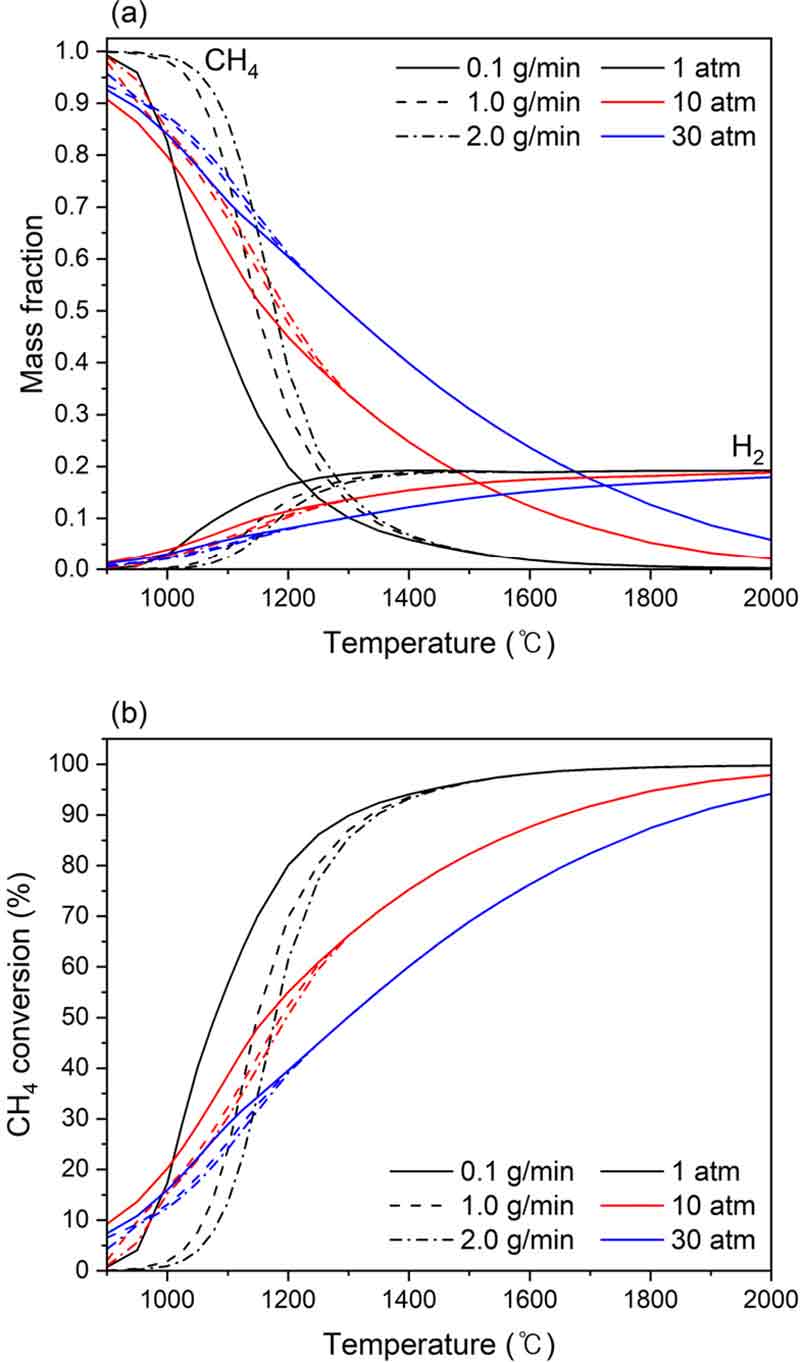
(a) Mass fraction of CH4 and H2, and (b) CH4 conversion with respect to temperatures, pressures, and methane flow rates
반면 동일 반응 온도 및 동일 메탄 유량 조건에서 압력이 증가할수록 반응기 출구에서의 메탄 질량 분율은 증가하였으며 수소 질량 분율은 감소하는 경향을 보였다. 또한 특징적으로 1 atm일 때 약 1,470℃, 10 atm일 때 약 1,300℃, 30 atm에서 약 1,220℃에서부터 메탄 유량에 따른 수소 질량 분율의 변화가 없었으며 압력이 증가할수록 특정 온도가 감소하였다. 따라서 동일 압력 조건에서 특정 온도는 메탄 유량에 대한 민감도가 없으며 압력이 낮을수록 메탄 유량에 따라 수렴 온도가 증가하므로 압력에 반비례한다.
Fig. 3(b)에서 압력이 증가할수록 메탄 전환율이 감소하는 경향을 보였다. 특히 메탄의 질량 분율에 대한 변화량이 큰 반응 온도 1,200℃에서 메탄 유량 0.1 g/min일 때 반응 압력 1 atm에서 최대 메탄 전환율이 80.09%로 예측되었으나 반응 압력 30 atm에서는 최대 메탄 전환율이 39.58%로 예측되었다. 이는 압력이 증가함에 따라 메탄 분해가 억제되어 메탄 전환율을 급격하게 감소시켜 메탄 전환율이 압력의 영향을 받은 것으로 판단된다.
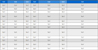
온도 및 압력에 따른 메탄 유량별 반응기 내부에서의 반응물 체류 시간을 예측한 결과를 Fig. 4에 나타내었다. Fig. 3(b)에서 동일 반응 압력 및 동일 반응 온도에서 메탄 유량이 감소할수록 메탄 전환율은 증가하는 경향을 보였다. 이는 Fig. 4의 체류 시간 결과에 따라 유량이 감소할수록 체류 시간이 증가하여 메탄 분해 시간이 확보됨에 따라 메탄 전환율이 증가한 것으로 판단된다. 또한 메탄 유량이 증가할수록 체류 시간이 감소하여 반응 시간이 축소되나 온도가 증가할수록 반응 속도 증가에 의한 메탄 전환 효과가 높아 체류 시간 변화에 대한 민감도가 낮아진다.
반면 압력이 증가함에 따라 체류 시간은 크게 증가함에도 불구하고 1,200℃ 이상의 고온 영역에서는 모든 메탄 유량 조건에서 1 atm 대비 낮은 메탄 전환율이 예측되었다. 반응 온도와 압력은 반응 속도와 연관된 매개변수로 Fig. 3의 결과를 통해 반응 온도가 증가함에 따라 반응 속도가 증가하나 압력이 높아질수록 온도 증가 효과가 감소하는 것을 알 수 있다. 이는 메탄 열분해 시 반응 속도가 증가하게 되고 수소 생성에 따라 생성물의 부피가 증가하게 되나 압력이 높아짐에 따라 생성물의 부피 증가가 억제되어 메탄 전환율이 감소한 것으로 판단된다. 따라서 메탄 열분해에서의 반응 온도 및 체류 시간은 메탄 전환율을 높이는 매개변수로 보이나 압력 증가에 따른 체류 시간 증가는 고온 영역에서의 효과가 미미한 것으로 예측되었다.
메탄의 열적 분해에 따른 수소 및 탄화수소로의 전환은 온도, 메탄 유량, 압력 등 다양한 매개변수에 의해 영향을 받는 것으로 예측되었다. Fig. 5는 1 atm 조건에서 메탄 유량 및 반응 온도에 따른 반응기 출구에서의 주요 화학종에 대한 질량 분율을 나타낸 것이다. Fig. 5(a)에서는 Fig. 3(b)에서 메탄 유량에 대한 메탄 전환율의 변화가 두드러진 반응 온도 1,200℃를 기준으로 하였으며 Fig. 5(b)에서는 메탄 유량 0.1 g/min을 기준으로 하였다.
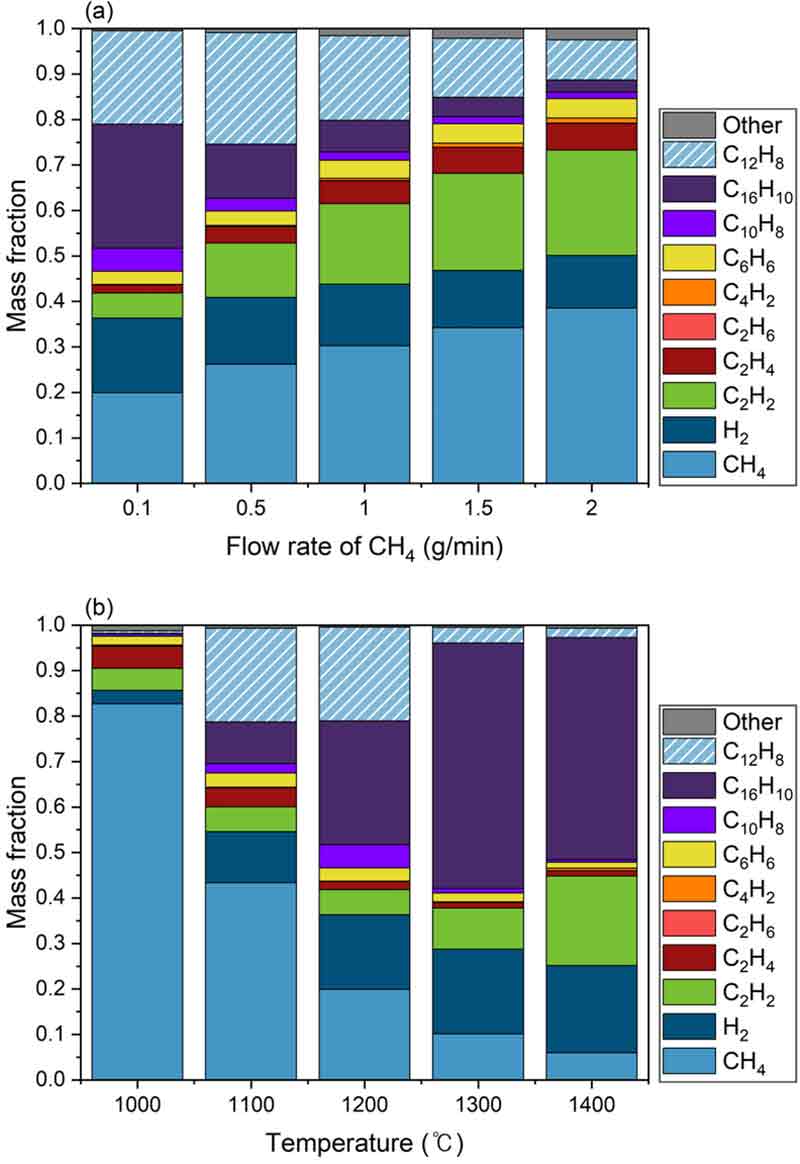
Mass fractions of major species with respect to (a) methane flow rates at 1 atm and 1,200℃ and (b) temperatures at 1 atm and 0.1 g/min
Fig. 5(a)에 도시된 바와 같이 1,200℃의 동일 반응 온도에서 메탄 유량이 증가할수록 메탄 잔류량이 증가하면서 생산되는 수소 질량 분율이 감소하였다. 메탄 유량이 증가하면 Fig. 4와 같이 체류 시간이 짧아지게 되며 CH4에서 H2로 전환하기 위한 반응 시간이 짧아 메탄 유량이 증가함에 따라 생성되는 수소 질량 분율이 감소한 것으로 예측된다. C2H2, C2H4, C6H6와 같이 주요 화학종의 생성량은 증가하였으나 C10H8, C16H10, C12H8과 같이 고분자 탄화수소의 생성량은 감소하는 경향을 보였다. 짧은 체류 시간으로 인하여 비교적 저분자 탄화수소의 합성이 증가하였으며 고분자 탄화수소로의 전환은 긴 체류 시간이 필요할 것으로 보인다.
Fig. 5(b)에서는 동일 메탄 유량일 때 온도가 증가할수록 메탄 전환율이 증가함(Fig. 3[b])에 따라 수소 및 C2H2의 질량 분율이 증가하였다. 또한 반응 온도가 1,200℃까지 증가하면서 C6H6, C10H8, C12H8의 질량 분율이 증가하였으나 반응 온도 1,300℃ 이상에서는 감소하는 경향을 보였다. 다만 반응 온도가 증가함에 따라 C16H10의 질량 분율이 증가하는 경향을 보였는데 이는 반응 온도가 증가할수록 탄소화가 가속화되는 것으로 판단된다.
Fig. 5를 통해 다양한 조건에서 메탄의 열적 전환을 통한 최종 생성물에 대한 거동을 예측하였다. 고온에 의하여 메탄이 분해되면서 수소가 생성되며 다양한 탄화수소가 부산물로 형성됨을 확인하였다. Fig. 6은 반응 온도 1,200℃ 및 1,400℃ 조건에서 메탄 유량에 따른 반응기 내부의 주요 화학종의 질량 분율 변화에 대한 예측 결과를 비교한 결과이다.
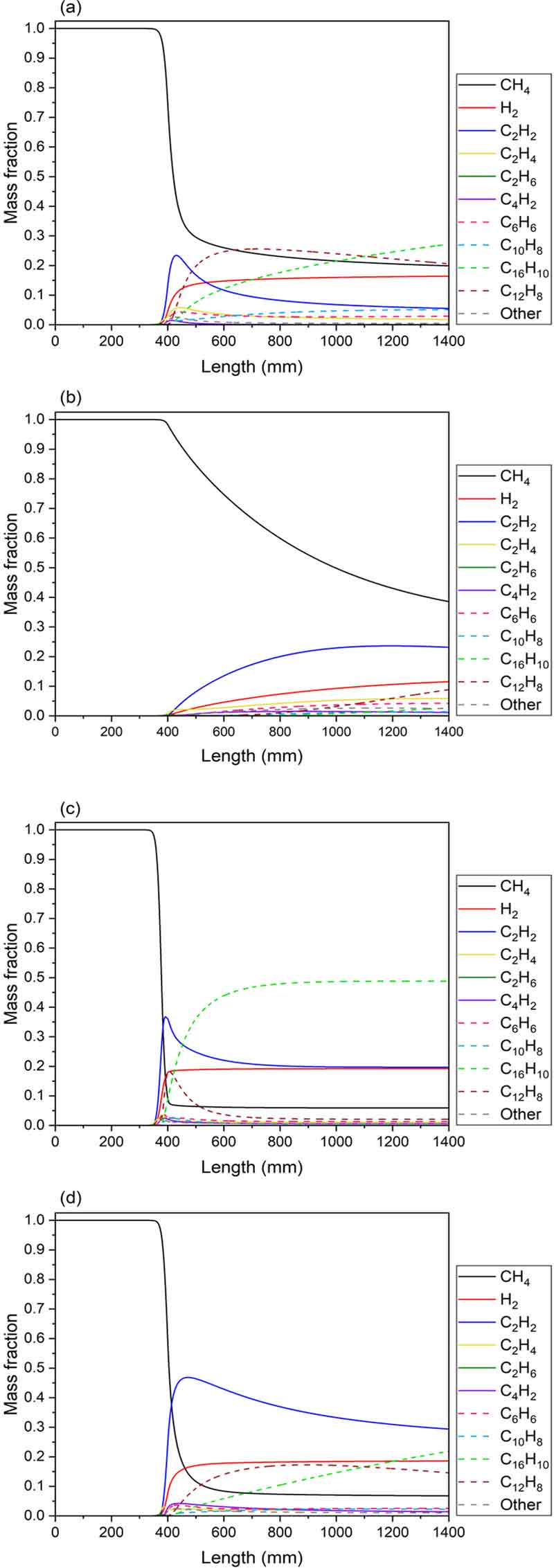
Mass fraction profiles of major species in terms of reactor length for methane flow rates of (a) 0.1 g/min and (b) 2.0 g/min at 1,200℃, (c) 0.1 g/min and (d) 2.0 g/min at 1,400℃
Fig. 6(a)에서는 메탄 분해가 진행됨에 따라 메탄 열분해 반응의 주요 화학종인 C2H2, C2H4, C6H6의 생성량이 증가하면서 수소 생성량이 증가하는 것을 볼 수 있다. 또한 C10H8, C16H10 및 C12H8과 같이 고분자 탄화수소의 생성량은 증가하고 C2H2는 감소하는 것을 볼 수 있는데 이는 탄소화가 진행되고 있는 것으로 판단된다. 반면 Fig. 6(b)에서는 메탄 유량이 2.0 g/min 으로 증가함에 따라 Fig. 4에 도시된 바와 같이 체류 시간이 감소하여 메탄 분해가 정상 상태(steady state)에 도달하지 못한 것을 확인하였다. 이에 따라 메탄 잔류량이 증가하였으며 수소 생성량도 감소하였다. 또한 Fig. 6(a)에서와 같이 C2H2의 감소가 미미하여 고분자 탄화수소로의 반응이 충분히 진행되지 못한 것으로 예측되었다.
Fig. 6(c) 및 Fig. 6(d)는 반응 온도 1,400℃에서 메탄 유량에 대한 변화를 적용한 결과이다. 반응 온도가 1,200℃에서 1,400℃로 증가함에 따라 메탄 유량의 변화와 무관하게 생성된 수소는 짧은 구간 내 정상 상태에 도달하였다. Fig. 6(c)를 보면 C2 분자, C4H2, C6H6가 생성됨에 따라 수소 생성량이 증가하였다. 여기서 C2 분자는 탄소 수가 2인 모든 화학종으로 C2H2, C2H4 및 C2H6를 의미한다. 반면 Fig. 6(d)에서는 Fig. 6(c)와 비교하여 메탄 유량이 2.0 g/min으로 증가하였음에도 불구하고 수소 생성량은 유사하나 C2H2, C4H2 및 C6H6의 생성량이 크게 증가하였다. 메탄 유량 0.1 g/min 조건에서 C12H8은 수소 생성과 동시에 분해되었으며 C16H10 생성량이 증가하다 정상 상태에 도달하였다. 메탄 유량 2.0 g/min 조건의 경우 C12H8, C16H10과 같이 고분자 탄화수소가 생성됨에 따라 탄소화 과정이 진행되는 것으로 예측되었다. 다만 모든 조건에서 반응이 진행되면서 탄화수소의 질량 분율은 증가하였으나 메탄 유량 2.0 g/min 조건에서 정상 상태에 도달하기 위한 체류 시간이 추가적으로 필요한 것으로 보인다.
동일 메탄 유량 조건에서는 반응 온도가 1,200℃에서 1,400℃로 증가함에 따라 정상 상태 도달 구간이 짧아질 것으로 예측되었다. 또한 반응 온도 1,400℃에서 메탄 잔류량이 감소하고 수소 생성량이 증가하였으며 특징적으로 C2H2, C16H10 생성량도 증가하였다. 반응 온도 1,200℃ 조건에 비해 1,400℃ 조건에서 C12H8의 생성량은 감소하였는데 C16H10의 생성량이 증가한 것으로 보아 C12H8의 탄소화에 따른 C16H10의 생성 반응이 이루어진 것으로 예측된다.
Fig. 6(b) 및 Fig. 6(d)의 경우 메탄 유량 2.0 g/min에서의 반응 온도에 대한 변화를 예측한 결과이다. 앞선 결과와 다르게 반응 온도 1,200℃ 조건에서는 정상 상태에 도달하지 못하였으나 반응 온도가 1,400℃로 증가함에 따라 메탄 잔류량이 감소하면서 Fig. 6(a)와 유사하게 높이 800 mm 지점부터 정상 상태에 도달하였다. 특히 C2 분자 및 C4H2는 고온일수록 생성량이 증가하였다. 또한 C12H8, C16H10과 같이 고분자 탄화수소는 생성량이 증가하나 체류 시간의 감소로 인한 탄소화 과정 시간이 짧은 것으로 해석된다.
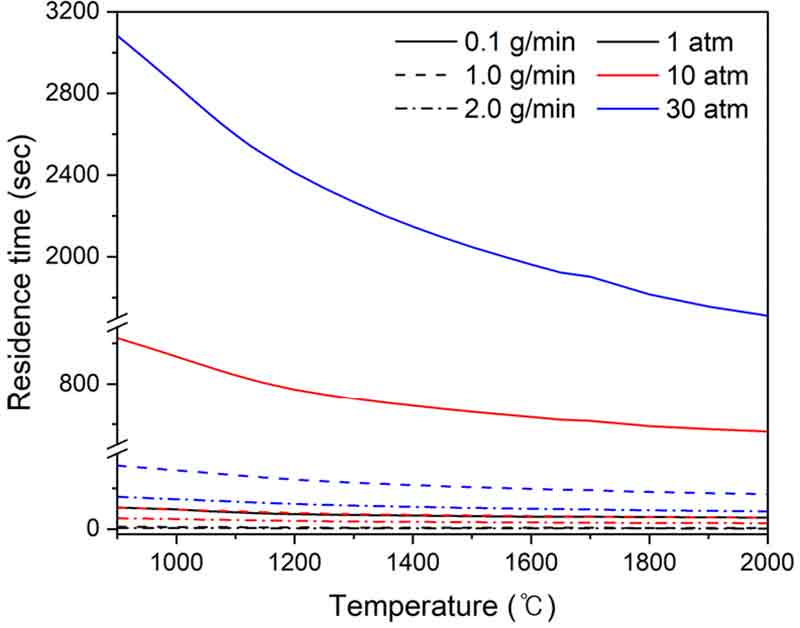
Fig. 7은 반응 온도 1,200℃, 메탄 유량 1.0 g/min일 때 반응 압력에 따른 반응기 출구에서의 주요 화학종의 질량 분율을 예측한 결과이다. Fig. 3에서 분석된 바와 같이 본 연구에서는 1,000℃ 이상의 반응 온도부터 메탄 열분해 반응이 진행되는 것을 알 수 있었다. 압력에 따른 주요 화학종 거동 분석을 위하여 화학 반응 변화량이 큰 1,200℃를 기준으로 선정하였으며 메탄 유량은 압력이 증가함에 따라 민감도가 감소하여 1.0 g/min을 기준으로 하였다.
Fig. 7에서 동일 반응 온도 및 동일 메탄 유량 조건에서 압력이 증가할수록 메탄 잔류량이 증가함에 따라 수소 질량 분율이 감소하였다. 이는 압력에 의하여 반응이 억제됨에 따라 수소 생성의 중간체 역할을 하는 C2 분자의 질량 분율이 감소하면서 수소 생산량이 감소한 것으로 판단된다. C10H8, C12H8과 같이 대부분의 고분자 탄화수소는 압력이 증가함에 따라 생성되는 질량 분율이 감소하였다. 다만 C16H10은 10 atm으로 압력이 증가하면서 일시적으로 증가하였으나 20 atm부터 감소하는 경향을 보였다. 압력이 증가할수록 저분자 탄화수소에 비해 고분자 탄화수소의 질량 분율에 대한 비율이 큰 것을 확인할 수 있다. 이는 압력의 증가로 인하여 메탄 전환율이 감소하며 메탄에서 탄소화되는 경로가 단순화되어 고분자 탄화수소의 생성 비율이 더 커진 것으로 예측된다.
Fig. 8은 반응 온도 1,200℃, 메탄 유량 1.0 g/min 조건에서 압력에 따른 반응기 내부에서 주요 화학종의 질량 분율 분포를 나타낸 결과이다. Fig. 8(a)에서 메탄이 분해되면서 수소 생성과 동시에 C2 분자 및 C12H8, C16H10과 같은 고분자 탄화수소가 생성되었다. 반면 Fig. 8(b), (c)에서 압력이 증가하면서 메탄 잔류량이 증가하였으나 Fig. 8(a)에 비해 비교적 정상 상태에 빠르게 도달하는 것을 볼 수 있다. 다만 메탄 잔류량의 증가로 인하여 상대적으로 적은 양의 수소가 생성되었다. 수소의 경우 C2 분자 및 C6H6가 증가할 때 수소 생성량이 정상 상태에 도달하는 것을 볼 수 있는데 이는 메탄에서 수소로의 전환에서 이들이 주요 화학종으로 작용한 것으로 예측된다. 또한 C16H10 생성량이 일시적으로 증가한 것은 압력이 증가하면서 메탄과 수소의 합성19) 및 C10H8, C12H8과 같은 고분자 탄화수소의 생성 및 분해로 인하여 발생한 것으로 예측된다.
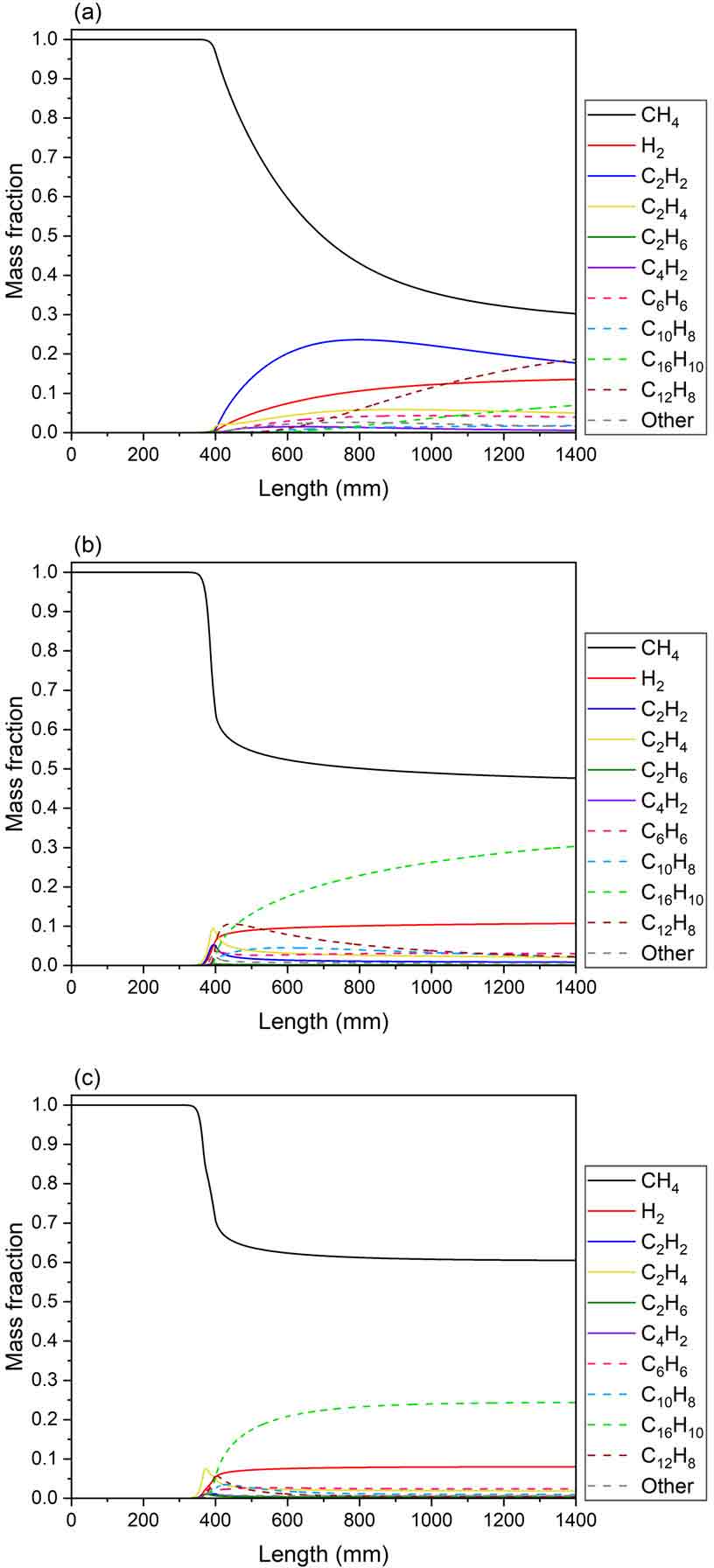
Mass fraction profiles of major species in terms of reactor length for pressures such as (a) 1 atm, (b) 10 atm, and (c) 30 atm at 1,200℃ and 1.0 g/min
특히 Fig. 8(c)에서 압력이 30 atm으로 급격하게 증가하면서 수소 및 대부분의 탄화수소 생성량이 감소하였다. 메탄 잔류량의 증가 및 수소 생성의 중간체인 C2 분자의 생성 억제로 인해 수소 질량 분율이 감소하였다. 또한 Fig. 8을 보면 고분자 탄화수소의 질량 분율이 증가하는 것을 확인할 수 있다. 이는 Fig. 7에 도시된 바와 같이 압력의 증가로 인하여 메탄 열분해 반응이 억제되었으며20) 메탄에서 고분자 탄화수소로의 반응률이 높아진 것으로 예측된다.
다음은 Fig. 8(a)에서 메탄 전환에 따른 탄화수소 생성에 관여된 주요 화학 반응을 나타낸 것으로 R21부터 R27까지는 C2H2 및 C2H4 형성에 관한 것이다. R21에서 1차 라디칼이 생성되며 라디칼의 합성 및 분해의 연쇄 반응에 의하여 C2H6, C2H5가 생성되며 C2H4를 형성한다. C2H4는 H 라디칼과 반응하여 C2H3가 생성되고 C2H3는 H 및 C2H2로 분해되는 것을 확인하였다.
R194 및 R222는 C12H8 생성의 주요 화학 반응을 나타낸 것이다. 메탄에 의해 생성된 C2H2는 C10H7과 합성되어 C12H9가 형성되고 C12H9는 열에 의하여 분해되어 H 라디칼 및 C12H8을 생성한다.
| (R21) |
| (R19) |
| (R36) |
| (R31) |
| (R32) |
| (R27) |
| (R194) |
| (R222) |
다음은 Fig. 8(c)에서 30 atm 조건에서의 메탄 전환에 따른 탄화수소 생성에 관여된 주요 화학 반응을 나타낸 것이다. Fig. 8에 도시된 바와 같이 동일 반응 온도 및 동일 메탄 유량 조건에서 30 atm으로 압력이 증가할 경우 대부분 탄화수소 생성량이 줄어들었으나 초기에 C2H4가 생성된 이후 C16H10이 생성되는 것을 확인할 수 있다. R21 반응을 통해 메탄이 열분해되어 1차 라디칼인 수소 및 CH3*를 생성하였으며 CH3*는 C2H6로 합성되었다. C2H6는 H 라디칼과 반응하여 수소 및 C2H5로 전환되었으며 C2H5는 분해되어 C2H4를 형성하였다.
R32, R27 및 R228은 C2H4가 C16H10으로 전환되는 과정을 나타낸 주요 화학 반응이다. 메탄이 분해되어 생성된 C2H4는 H 라디칼과 반응하여 수소 및 C2H3를 생성하였으며 C2H3는 분해되어 C2H2를 형성하였다. C2H2는 C14H9과 합성하여 최종적으로 C16H10을 생성하였다.
| (R21) |
| (R19) |
| (R36) |
| (R31) |
| (R32) |
| (R27) |
| (R228) |
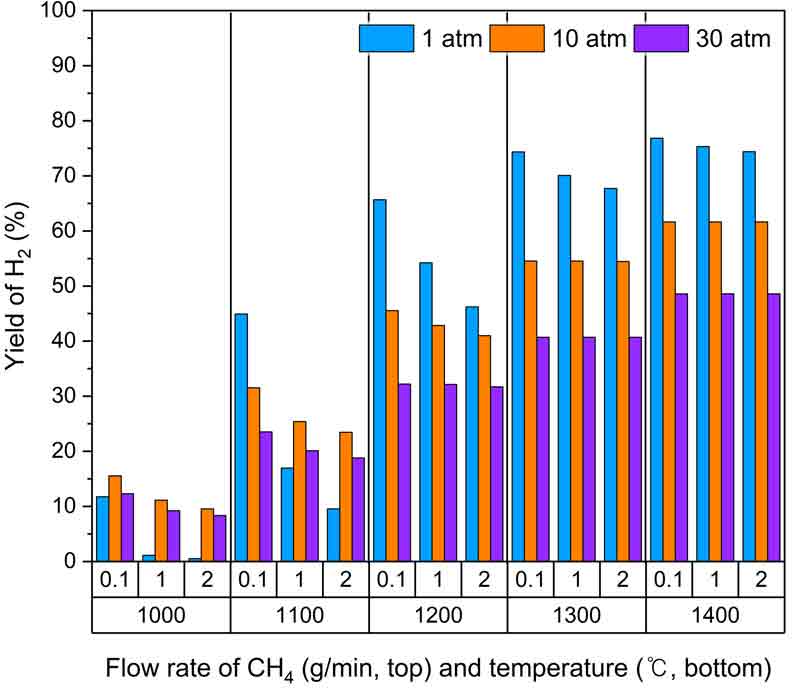
Fig. 9는 반응기 출구에서의 온도 및 메탄 유량에 따른 압력별 수소 수율을 예측한 결과이다. 온도가 증가할수록, 메탄 유량이 감소할수록 최대 수소 수율이 증가하는 것을 확인할 수 있다. 이는 온도가 증가함에 따라 메탄의 열화학적 전환에 의하여 메탄 질량 분율이 크게 감소하였으며 수소 질량 분율이 증가한 것으로 예측되었다. 또한 Fig. 4의 체류 시간 결과에 의하면 CH4에서 H2로 전환되는 체류 시간이 증가함에 따라 수소 생성량이 증가하는 것으로 판단된다.
Fig. 9를 보면 동일 메탄 유량 조건에서 1,200℃까지 압력이 증가할수록 수소 수율에 대한 경향이 일정하지 않으며 반응 온도 1,000-1,100℃, 메탄 유량 1.0 g/min 이상에서는 압력이 1 atm 초과 조건에서 수소 수율이 높게 예측되었다. 반면 반응 온도 1,300℃ 이상 조건에서는 1 atm 초과 조건에서 메탄 유량과 무관하게 최대 수소 수율이 유사한 것을 확인하였다. Fig. 7에 의해 압력이 증가할수록 메탄 잔류량이 증가함에 따라 생성되는 수소 질량 분율의 차이가 크지 않은 것을 알 수 있다. 또한 Fig. 8의 동일 메탄 유량 조건에서 압력이 증가할수록 고분자 탄화수소의 합성으로 인한 탄소화가 진행되어 압력의 영향으로 수소 및 저분자 탄화수소의 질량 분율이 감소하여 수소 수율이 유사하게 나타나는 것으로 판단된다. 특정 반응 온도 구간에서는 메탄 유량과 압력에 따라 수소 수율 경향이 차별적으로 예측되었기에 반응 온도 및 메탄 유량에 따라 압력을 선택적으로 고려할 필요가 있을 것이다.
4. 결 론
본 연구에서는 메탄 열분해 모사를 위한 화학 반응 기구를 검증하고 이를 적용하여 1차원 PFR 수치해석을 통해 매개변수에 따른 메탄 열분해 생성물의 거동을 예측, 분석하고자 수행되었으며 이를 통해 메탄 열분해에 따른 수소 생성 거동 및 수소 수율 증대를 위한 주요 매개변수를 평가하였다.
Hamdullahpur에 의해 제안된 화학 반응 기구는 실험과의 비교를 통해 오차율 10% 이내의 예측도를 보였기에 메탄 열분해 모사에 적정한 화학 반응 기구임을 검증하였으며 이를 활용한 매개변수별 민감도를 조사하고 분석하였다.
반응 온도가 증가할수록, 메탄 유량이 감소할수록 반응 속도 및 시간 증가로 메탄 전환율 및 수소 생성량이 증가하였다. 반면 수렴 온도 이상에서는 체류 시간 감소에 따른 반응 시간 효과 대비 온도 증가에 따른 반응 속도 증가 효과가 큰 것으로 보인다.
압력이 증가할수록 메탄 분해가 억제되어 메탄 잔류량이 증가함에 따라 수소 생성량이 감소하는 경향을 보였다. 또한 특정 조건에서는 높은 압력에서 최대 수소 수율이 유사한 것을 확인하였는데 이는 고분자 탄화수소의 합성으로 인한 탄소화가 진행되는 것으로 판단된다.
종합적으로 수소 수율을 증대하기 위해서 반응 온도 증가, 메탄 유량 감소 및 압력 감소가 중요한 것으로 예측되었다. 또한 전반적인 매개변수 영역에서는 메탄 열분해 반응에서 온도 및 메탄 유량이 주요 매개변수인 것으로 판단되나 특정 영역에서는 압력이메탄 유량 및 온도 대비 수소 수율을 높이는 선택적 주요 매개변수로 고려될 수 있음을 확인하였다. 향후 본 연구에서 평가된 반응 온도, 메탄 유량 그리고 압력에 대한 실험과의 비교, 검증 연구가 수행될 필요가 있을 것이다.
Acknowledgments
본 연구는 2024년도 정부(과학기술정보통신부)의 재원으로 한국연구재단-석유대체 친환경 화학기술개발사업(No. 2022M3J5A1051728)의 일환으로 수행되었으며 이에 감사드립니다. 본 연구는 2024년도 정부(과학기술정보통신부)의 재원으로 국가과학기술연구회 창의형 융합연구사업(No. CAP22023-000)의 지원을 받아 수행되었습니다.
References
-
S. Dermühl and U. Riedel, “A comparison of the most promising low-carbon hydrogen production technologies”, Fuel, Vol. 340, 2023, pp. 127478.
[https://doi.org/10.1016/j.fuel.2023.127478]

-
S. Schneider, S. Bajohr, F. Graf, and T. Kolb, “State of the Art of hydrogen production via pyrolysis of natural gas”, Chemie Ingenieur Technik, Vol. 92, No. 8, 2020, pp. 1023-1032.
[https://doi.org/10.1002/cite.202000021]

-
J. Kim, C. Oh, H. Oh, Y. Lee, H. Seo, and Y. K. Kim, “Catalytic methane pyrolysis for simultaneous production of hydrogen and graphitic carbon using a ceramic sparger in a molten NiSn alloy”, Carbon, Vol. 207, 2023, pp. 1-12.
[https://doi.org/10.1016/j.carbon.2023.02.053]

-
X. Hu, Y. Hu, Q. Xu, X. Wang, G. Li, H. Cheng, X. Zou, and X. Lu, “Molten salt-promoted Ni–Fe/Al2O3 catalyst for methane decomposition”, International Journal of Hydrogen Energy, Vol. 45, No. 7, 2020, pp. 4244-4253.
[https://doi.org/10.1016/j.ijhydene.2019.11.209]

-
M. Mokashi, A. B. Shirsath, P. Lott, H. Müller, S. Tischer, L. Maier, and O. Deutschmann, “Understanding of gas-phase methane pyrolysis towards hydrogen and solid carbon with detailed kinetic simulations and experiments”, Chemical Engineering Journal, Vol. 479, 2024, pp. 147556.
[https://doi.org/10.1016/j.cej.2023.147556]

-
F. Carretta, S. Pelucchi, F. Galli, and P. Mocellin, “Methane pyrolysis for hydrogen production: modeling of soot deposition by computational fluid dynamics and experimental validation”, Chemical Engineering Journal, Vol. 485, 2024, pp. 149844.
[https://doi.org/10.1016/j.cej.2024.149844]

-
A. Khrabry, I. D. Kaganovich, Y. Barsukov, S. Raman, E. Turkoz, and D. Graves, “Compact and accurate chemical mechanism for methane pyrolysis with PAH growth”, International Journal of Hydrogen Energy, Vol. 56, 2024, pp. 1340-1360.
[https://doi.org/10.1016/j.ijhydene.2023.12.175]

-
L. Chen, S. Pannala, B. Nair, I. Lengyel, B. Baek, C. Wu, R. Vm, and D. West, “Experimental and numerical study of a two-stage natural gas combustion pyrolysis reactor for acetylene production: the role of delayed mixing”, Proceedings of the Combustion Institute, Vol. 37, No. 4, 2019. pp. 5715-5722.
[https://doi.org/10.1016/j.proci.2018.05.170]

-
G. Fau, N. Gascoin, P. Gillard, and J. Steelant, “Methane pyrolysis: literature survey and comparisons of available data for use in numerical simulations”, Journal of Analytical and Applied Pyrolysis, Vol. 104, 2013, pp. 1-9.
[https://doi.org/10.1016/j.jaap.2013.04.006]

-
A. S. Gordon, “Pyrolysis of methane flowing through a porcelain tube in the region 1000℃”, Journal of the American Chemical Society, Vol. 70, No. 1, 1948, pp. 395-401.
[https://doi.org/10.1021/ja01181a125]

-
F. Billaud, C. Gueret, and J. Weill, “Thermal decomposition of pure methane at 1263 K. Experiments and mechanistic modelling”, Thermochimica Acta, Vol. 211, 1992, pp. 303-322.
[https://doi.org/10.1016/0040-6031(92)87029-A]

- H. Jang, B. G. Lee, and J. S. Lim, “Production of hydrogen and carbon black using natural gas thermal decomposition method”, Clean Technology, Vol. 10, No. 4, 2004, pp. 203-213. Retrieved from https://www.dbpia.co.kr/journal/articleDetail?nodeId=NODE01975923, .
-
M. Y. Sinaki, E. A. Matida, and F. Hamdullahpur, “Development of a reaction mechanism for predicting hydrogen production from homogeneous decomposition of methane”, International Journal of Hydrogen Energy, Vol. 36, No. 4, 2011, pp. 2936-2944.
[https://doi.org/10.1016/j.ijhydene.2010.12.002]

-
A. Kéromnès, W. K. Metcalfe, K. A. Heufer, N. Donohoe, A. K. Das, C. J. Sung, J. Herzler, C. Naumann, P. Griebel, O. Mathieu, M. C. Krejci, E. L. Petersen, W. J. Pitz, and H. J. Curran, “An experimental and detailed chemical kinetic modeling study of hydrogen and syngas mixture oxidation at elevated pressures”, Combustion and Flame, Vol. 160, No. 6, 2013, pp. 995-1011.
[https://doi.org/10.1016/j.combustflame.2013.01.001]

- G. P. Smith, D. M. Golden, M. Frenklach, N. W. Moriarty, B. Eiteneer, M. Goldenberg, C. T. Bowman, R. K. Hanson, S. Song, W. C. Gardiner Jr, V. V. Lissianski, and Z. Qin, “GRI-Mech 3.0”, GRI-Mech, 1999. Retrieved from http://combustion.berkeley.edu/gri-mech/version30/text30.html, .
-
A. A. Konnov, “On the role of excited species in hydrogen combustion”, Combustion and Flame, Vol. 162, No. 10, 2015, pp. 3755-3772.
[https://doi.org/10.1016/j.combustflame.2015.07.014]

-
C. K. Westbrook, W. J. Pitz, O. Herbinet, H. J. Curran, and E. J. Silke, “A comprehensive detailed chemical kinetic reaction mechanism for combustion of n-alkane hydrocarbons from n-octane to n-hexadecane”, Combustion and Flame, Vol. 156, No. 1, 2008, pp. 181-199.
[https://doi.org/10.1016/j.combustflame.2008.07.014]

-
P. Y. Dou, W. W. Yang, X. Y. Tang, X. Ma, and J. C. Li, “Topology optimization of catalyst bed structure for a solar steam methane reforming reactor aiming at improved conversion efficiency and hydrogen yield”, Chemical Engineering Science, Vol. 281, 2023, pp. 119200.
[https://doi.org/10.1016/j.ces.2023.119200]

-
W. Tao, Y. R. Zou, A. Carr, J. Liu, and P. Peng, “Study of the influence of pressure on enhanced gaseous hydrocarbon yield under high pressure-high temperature coal pyrolysis”, Fuel, Vol. 89, No. 11, 2010, pp. 3590-3597.
[https://doi.org/10.1016/j.fuel.2010.06.007]

-
M. R. G. Pangestu, Z. Malaibari, A. Muhammad, F. N. Al-Rowaili, and U. Zahid, “Comprehensive review on methane pyrolysis for sustainable hydrogen production”, Energy & Fuels, Vol. 38, No. 15, 2024, pp. 13514-13538.
[https://doi.org/10.1021/acs.energyfuels.4c01551]