Fe/Cr 촉매 펠릿을 이용한 고온 수성가스 전환 반응
2025 The Korean Hydrogen and New Energy Society. All rights reserved.
Abstract
Fe/Cr catalyst pellet was prepared for the high temperature water gas shift reaction (HTWGSR) to produce H2 gas from the gasified gases of waste plastics. The Fe/Cr catalyst pellet was synthesized using a compression molding method with the prepared catalyst powders. The HTWGSR was conducted using the prepared catalyst pellet with CO:H2O ratios of 1:2 to 1:4 at a temperature range of 300-400℃. The maximum average CO conversion was observed at a CO:H2O ratio of 1:3, with a value of 96.5% at 300℃, at CO:H2O ratios of 1:3 and 1:4, with a value of 96.7% at 350℃, and at a CO:H2O ratio of 1:4, with a value of 95% at 400℃. It is considered that a CO:H2O ratio of 1:3 at 300℃ and 350℃, and a CO:H2O ratio of 1:4 at 400℃, are suitable for high temperature water gas shift reactions in terms of CO conversion.
Keywords:
Waste plastic gasification, Water gas shift reaction, Hydrogen production, Catalyst, Catalyst pellet키워드:
폐플라스틱 가스화, 수성가스 전환 반응, 수소 제조, 촉매, 촉매 펠릿1. 서 론
플라스틱은 다양한 특성으로 인하여 여러 용도로 사용되고 있다. 그러나 사용된 플라스틱 대부분은 재활용되지 않고 폐기되기 때문에 폐플라스틱의 처리에서 여러 문제점이 대두되고 있다. 폐플라스틱을 매립지에 매립하는 방법은 수질 오염으로 인해 비환경적이고1) 소각에 의한 폐플라스틱의 처리는 지구 환경 오염 물질인 이산화탄소를 배출한다는 단점이 있다2). 그리고 플라스틱의 낮은 분해성은 해양 환경에서 심각한 환경 문제를 일으키고 있다3,4). 따라서 폐플라스틱의 관리가 시급히 해결해야 할 과제로 대두되고 있다.
최근에는 폐플라스틱을 다른 제품으로 전환하는 기술이 많은 관심을 받고 있다5-7). 특히 폐플라스틱을 에너지 운반체로 전환하는 열분해와 가스화 기술이 관심을 받고 있다2). 폐플라스틱의 가스화는 플라스틱 폐기물을 약 700-1,500℃의 고온에서 산소 및 공기와 반응시켜 H2, CO, CO2, CH4 가스 등을 생산한다. 폐플라스틱의 가스화 공정은 생성된 H2와 CO의 합성가스(syngas)로부터 합성 석유, dimethyl ether, 메탄올 등과 같은 연료와 수소와 같은 에너지 운반체를 생산하는 데 초점이 맞춰져 있다8).
합성가스로부터 고순도의 수소를 생산하기 위해서는 CO를 CO2로 전환하면서 수소를 추가로 생산하는 수성가스 전환(water gas shift, WGS) 반응이 필수적이다.
WGS 반응은 다음과 같이 진행되며 약간의 발열반응이고 평형상수는 온도가 증가함에 따라 감소한다.
| (1) |
일반적으로 WGS 반응은 발열반응과 가역반응이라는 주요 특성 때문에 CO 전환과 CO를 이용한 수소 생산을 선호한다. 하지만 반응속도의 한계 때문에 낮은 온도에서는 생산량이 감소한다. 따라서 상업적 응용에서는 2단계 공정을 사용하여 높은 반응속도와 높은 CO 전환을 동시에 달성하고자 한다9). 상업적 응용에서 WGS 반응은 열역학적 평형을 고려하여 높은 온도에서 빠른 반응속도로 수소를 생산하고 낮은 온도에서 추가로 반응시켜 최대의 수소를 생산하고자 300-500℃에서의 고온 수성가스 전환 반응(high temperature water gas shift reaction, HTWGSR)과 150-250℃에서의 저온 수성가스 전환 반응(low temperature water gas shift reaction)의 두 단계 공정으로 이루어진다9-12).
HTWGSR에서 촉매의 비활성화를 개선하고 CO 전환율을 증가시키기 위하여 많은 촉매 연구가 진행되고 있다13-19). 일반적으로 WGS 반응에서 CO:H2O 비율이 중요한 변수로 작용하며 CO:H2O 비율이 1:1 이하로 낮은 경우 HTWGSR용 촉매인 Fe 계열의 촉매에서는 금속 철의 형성, 메탄화, 탄소 침착 및 Fisher-Tropsch 반응 등이 일어나 CO 전환율이 낮은 것으로 알려져 있다11). 따라서 Fe 계열 촉매의 경우 CO:H2O 비율이 1:2 이상인 경우 CO 전환율에 관한 연구가 필요하다.
본 연구에서는 HTWGSR에 사용하기 위하여 Fe/Cr의 촉매 분말을 공침법으로 제조하고 제조한 촉매 분말을 고압 압축 성형하여 Fe/Cr 촉매 펠릿을 제조하였다. 그리고 제조한 촉매 펠릿을 사용하여 300-400℃에서 HTWGSR을 진행하여 CO:H2O의 비율에 따른 CO 가스 전환율을 평가하였다.
2. 실 험
2.1 Fe/Cr 촉매 분말의 제조
Fe/Cr 촉매 분말은 공침법에 의하여 제조되었다. 1 M Fe(NO3)3·9H2O (98.5%; Samchun Chemicals, Seoul, Korea), 1 M Cr(NO3)3·9H2O (98%; Samchun Chemicals)를 Fe:Cr의 중량비 70:30으로 하여 연속 교반하면서 혼합하였다. 이어서 1 L의 2 M NaOH 용액을 70℃에서 4시간 동안 연속 교반하면서 첨가하여 pH가 7.0±0.5로 유지되도록 하였다. 생성된 공침물을 실온에서 1시간 동안 숙성하였다. 얻어진 침전물을 진공 여과기를 이용하여 여과하고 증류수로 세척한 후 100℃에서 24시간 동안 건조하여 부산물과 미반응 물질을 제거하였다. 건조된 생성물을 분말로 분쇄하고 212-mesh체로 체질하여 균일한 입자를 얻었다. 체질한 분말을 공기 분위기에서 머플로를 이용하여 350℃에서 4시간 동안 소결하여 Fe/Cr 촉매 분말을 얻었다.
2.2 Fe/Cr 촉매 펠릿의 제조
Fe/Cr 촉매 분말을 α-terpineol에 용해한 후 폴리에틸렌 글리콜(polyethylene glycol, Junsei Chemical, Tokyo, Japan)을 바인더로 첨가하고 이 혼합물을 실온에서 300 rpm으로 1시간 동안 볼 밀링하여 촉매 슬러리를 얻었다. 촉매 분말:용매:바인더의 중량비는 20:1:1로 하였다. 다음으로 성형기를 사용하여 제조된 촉매 슬러리를 40 MPa의 압력으로 15분 동안 압축하여 원통형 펠릿을 제조하였다. 제조된 원통형 펠릿을 공기 분위기에서 머플로를 이용하여 600℃에서 4.83시간 동안 소결하여 원통형 Fe/Cr 촉매 펠릿(외경 약 6mm, 길이 약 5.5mm)을 얻었다.
2.3 Fe/Cr 촉매 분말과 촉매 펠릿의 특성 분석
제조한 촉매 분말의 결정 구조는 X선 회절(X-ray diffraction, XRD)을 사용하여 분석하였다. XRD 패턴은 Cu-ka 방사선과 Ni 필터를 사용하여 고니오미터 모드(goniometer mode)에서 작동하는 Empyrean (Malvern Panalytical BV, Almelo, Netherlands)을 사용하여 얻었다. 회절 각도는 10° [2θ]와 90° [2θ] 사이에서 측정하였다. 제조한 촉매 펠릿의 표면 형태와 원소 조성은 각각 주사 전자 현미경(scanning electron microscopy [SEM], FEI Company, Hillsboro, OR, USA)과 에너지 분산 X선 분광법(energy dispersive X-ray spectroscopy [EDXS], Oxford Instruments, Abingdon, UK)을 사용하여 분석하였다. 그리고 제조한 촉매 펠릿의 표면적과 기공 직경은 가스 흡착법(Brunauer-Emmett-Teller [BET], Quantachrome Corporation, Boynton Beach, FL, USA)을 사용하여 측정하였다. 또한 제조한 촉매 펠릿의 압축 강도는 압축 강도 측정기(compression strength tester [CST], TEST ONE, Busan, Korea)를 사용하여 측정하였다.
2.4 HTWGSR
Fig. 1은 HTWGSR의 실험 장치를 나타낸다.
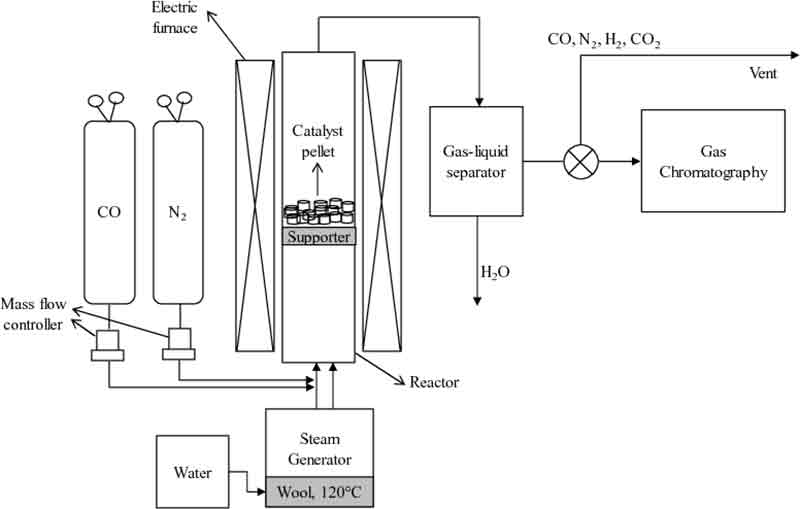
Experimental apparatus for the high temperature water gas shift reaction using the prepared catalyst pellet
원통형 stainless steel (SUS) 반응기(내경 34 mm, 길이 300 mm)를 Fig. 1과 같이 전기로 안에 설치하였다. 제조한 촉매 펠릿을 원통형 반응기의 SUS 지지대 위에 올려 약 3.16 mL의 부피가 되도록 하였다. 혼합가스(CO, H2O, N2)를 약 528 mL/min의 유량으로 반응기 안으로 흘려주었다. 수증기는 120℃의 증기발생기에 의해 공급되며 유량은 약 311 mL/min이었다. CO의 유량은 CO:H2O의 비율이 1:2, 1:3, 1:4가 되도록 조절하였으며 나머지 유량은 N2 가스를 이용하여 혼합가스 유량이 되도록 하였다. 혼합가스 유량을 촉매 펠릿의 부피로 나누어 계산한 가스 시간당 공간속도(gas hourly space velocity, GHSV)는 약 10,000 h-1이었다. HTWGSR은 상압(1 bar)과 300℃, 350℃, 400℃에서 70분 동안 진행하였다.
HTWGSR에서 생성된 CO2, H2 가스와 CO, N2를 포함한 가스는 가스 크로마토그래피(gas chromatography [GC], ChroZen; YOUNG IN Chromass, Anyang, Korea)를 사용하여 분석하였다. GC 분석을 위하여 취한 샘플은 0.25 mL였다. 각 가스에 대한 분석은 검량 곡선을 작성한 후에 진행하였다. 얻어진 GC 데이터를 기반으로 식 (2)를 사용하여 CO 전환율을 계산하였다.
| (2) |
3. 결과 및 고찰
3.1 Fe/Cr 촉매 분말과 촉매 펠릿의 특성 분석
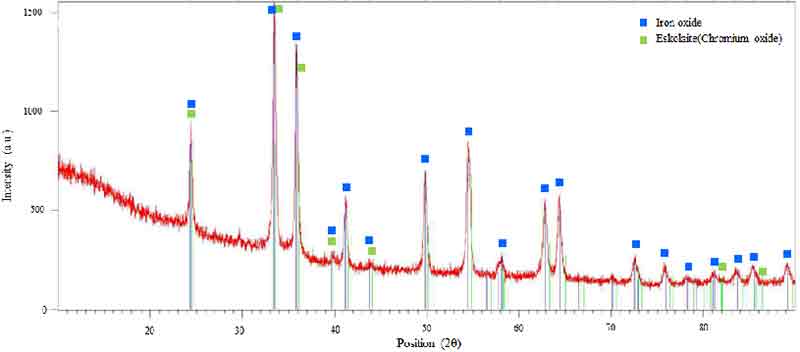
Fig. 2는 Fe/Cr 촉매 분말의 XRD 분석 결과를 나타낸다. XRD 분석에서 얻은 피크는 Joint Committee on Powder Diffraction Standards 카드에 의해 식별 및 분석되었다.
Fig. 2에서 볼 수 있듯이 제조한 Fe/Cr 촉매 분말의 XRD 패턴은 산화철(Fe2O3)과 산화크로뮴(Cr2O3) 상에 해당하는 두 개의 피크를 나타냈다. XRD 분석으로부터 제조한 Fe/Cr 촉매 분말은 Fe와 Cr의 산화물이 서로 결합한 상태인 것을 확인할 수 있었다.
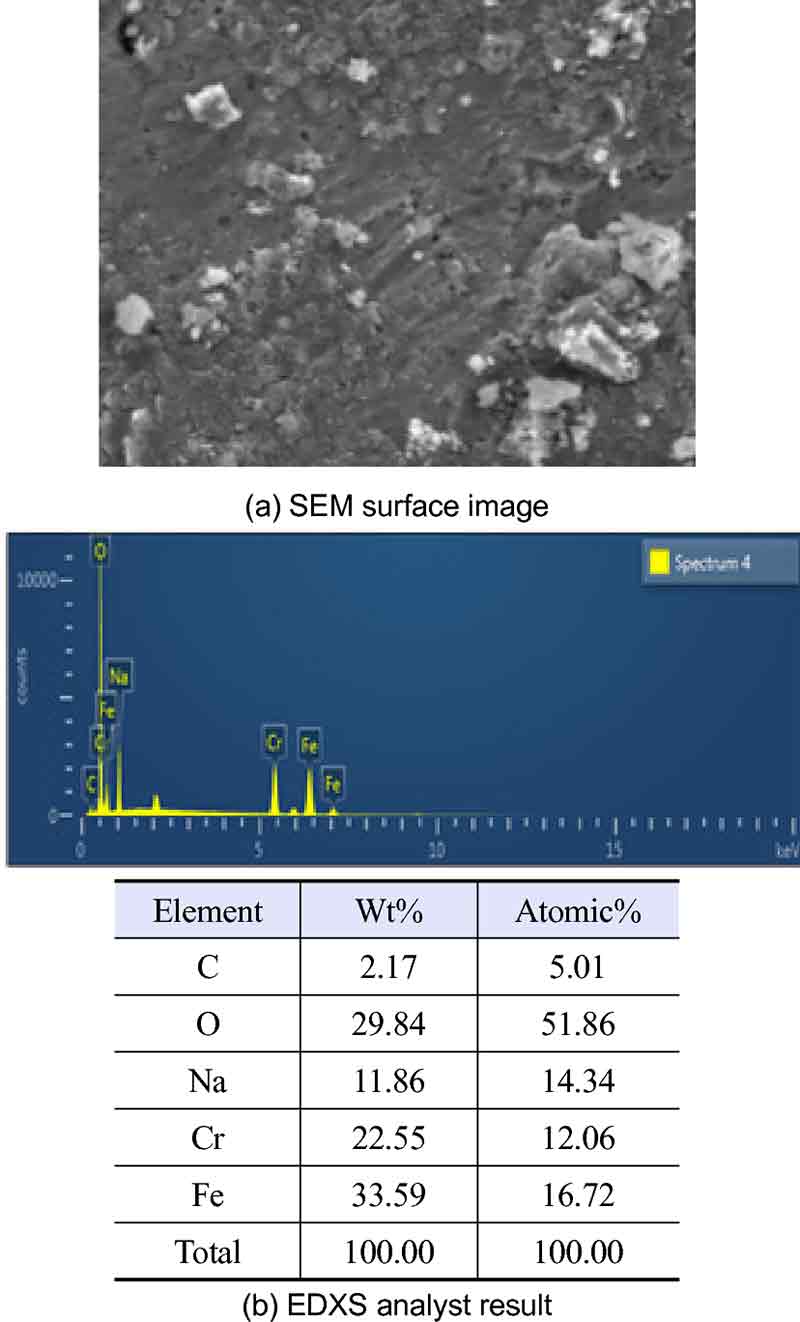
Fig. 3은 제조한 Fe/Cr 촉매 펠릿의 SEM 표면 사진과 EDXS 분석 결과를 나타낸다.
Fig. 3(a)의 SEM 표면 사진을 보면 알 수 있듯이 제조한 Fe/Cr 촉매 펠릿의 표면은 기공이 없는 것을 확인할 수 있었다. 이는 고압으로 압착하여 분말이 치밀하게 뭉쳐졌기 때문으로 판단된다.
Fig. 3(b)의 EDXS의 분석 결과를 보면 알 수 있듯이 Fe:Cr의 중량 퍼센트 비율은 33.59:22.55를 나타내고 있다. 이 비율을 단지 Fe와 Cr만의 중량 퍼센트 비율로 다시 환산하면 Fe:Cr은 60:40이었다. 이 비율은 촉매 분말을 제조할 때 Fe:Cr의 중량 비율인 70:30과는 약간 다른 결과를 보여주고 있다. 이러한 차이는 Fe와 Cr의 전구체를 혼합할 때 발생한 오류에 의한 것으로 판단된다. 또한 EDXS 분석 결과 Na 원소가 검출되었다. 이는 공침법으로 촉매를 제조할 때 pH를 맞추기 위하여 사용하는 NaOH 일부가 반응 후 세척 과정에서 완전히 제거되지 않았기 때문으로 판단된다. EDXS 분석으로부터 제조한 Fe/Cr 촉매 펠릿은 Fe와 Cr 원소를 함유하고 있음을 확인할 수 있었다.
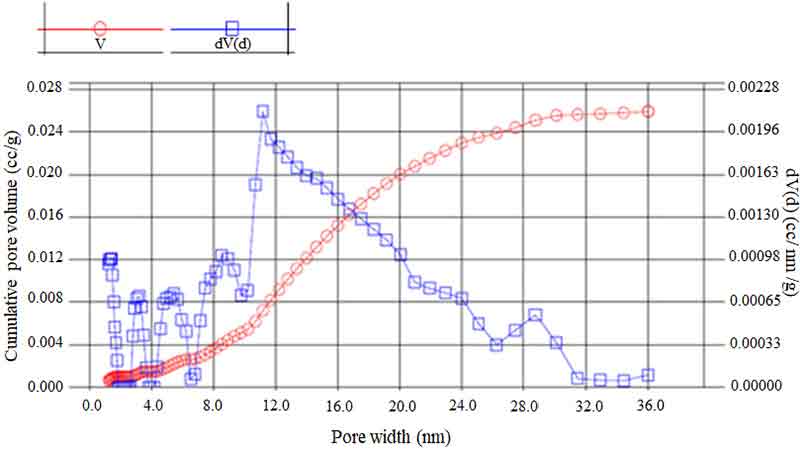
Fig. 4는 Fe/Cr 촉매 펠릿의 BET 분석 결과를 나타낸다.
BET 분석 결과 제조한 Fe/Cr 촉매 펠릿의 표면적은 5.88 m2/g, 기공 직경은 11.17 nm, 기공 부피는 0.026 mL/g이었다. 제조한 Fe/Cr 촉매 분말의 표면적은 34.82 m2/g, 기공 직경은 4.912 nm, 기공 부피는 0.12 mL/g이었다.
촉매 분말을 촉매 펠릿으로 제조할 때 표면적과 기공 부피가 감소하였다. 촉매 분말의 경우 HTWGSR에서 분말의 큰 입자 크기와 작은 표면적은 촉매 활성을 감소시키고 CO 전환율을 낮추는 것으로 알려져 있다20). 그러나 촉매 펠릿의 기공 구조가 HTWGSR에 미치는 영향은 아직 밝혀지지 않았다. 따라서 압축 성형 시 가해지는 압력에 의하여 촉매 펠릿의 기공 구조가 어떻게 변화하는지, 이러한 변화가 HTWGSR에 어떤 영향을 미치는지에 대한 추가 연구가 필요할 것으로 보인다.
Table 1은 제조한 Fe/Cr 촉매 펠릿과 상용 Fe/Cr 촉매 펠릿의 압축 강도를 나타낸다.
제조한 Fe/Cr 촉매 펠릿의 압축 강도는 7.56 MPa을, 상용 Fe/Cr 촉매 펠릿의 압축 강도는 6.60 MPa을 보였다. 이 결과로부터 제조한 촉매 펠릿은 상용 촉매 펠릿과 비교하여 동등 이상의 압축 강도를 가지고 있으며 높은 기계적 내구성을 보일 것으로 판단된다.
3.2 HTWGSR
Fig. 5는 제조한 Fe/Cr 촉매 펠릿을 이용한 HTWGSR의 각 온도에서 CO:H2O 비율에 따른 반응 시간과 N2 가스를 제외한 각 생성 가스 비율과의 관계를 나타낸다.
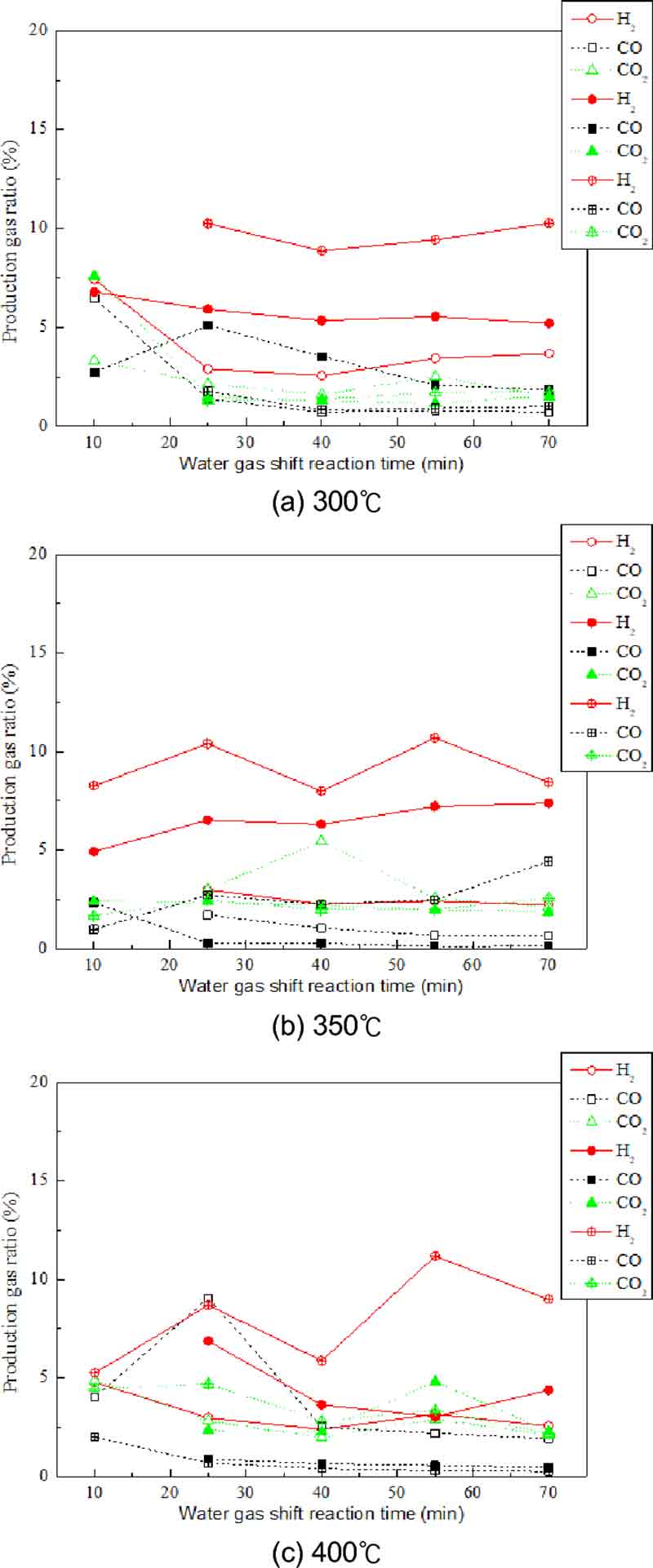
Relationship between reaction time and production gas ratio except N2 gas for each CO:H2O ratio and temperature during HTWGSR using Fe/Cr catalyst pellet (open symbol: CO:H2O=1:2, close symbol: CO:H2O=1:3, cross symbol: CO:H2O=1:4)
300℃의 HTWGSR에서 CO:H2O의 비율이 1:2인 경우 생성 가스 중 H2 가스의 비율은 반응 시간 10분 후 7.4%를, 70분 후 3.7%를 보였다. 반응 가스인 CO 가스의 비율은 반응 시간 10분 후 6.5%를, 70분 후 0.7%를 보였다. 또한 생성 가스 중 CO2 가스의 비율은 반응 시간 10분 후 3.3%를, 70분 후 1.5%를 보였다. CO:H2O의 비율이 1:3인 경우 H2 가스의 비율은 반응 시간 10분 후 6.8%를, 70분 후 5.2%를 보였다. CO 가스의 비율은 반응 시간 10분 후 2.7%를, 70분 후 1.8%를 보였다. 또한 CO2 가스의 비율은 반응 시간 10분 후 7.6%를, 70분 후 1.5%를 보였다. CO:H2O의 비율이 1:4인 경우 H2 가스의 비율은 반응 시간 25분 후 10.2%를, 70분 후 10.3%를 보였다. CO 가스의 비율은 반응 시간 10분 후 1.8%를, 70분 후 1.0%를 보였다. 또한 CO2 가스의 비율은 반응 시간 10분 후 1.3%를, 70분 후 1.7%를 보였다.
350℃의 HTWGSR에서 CO:H2O의 비율이 1:2인 경우 생성 가스 중 H2 가스의 비율은 반응 시간 25분 후 3.0%를, 70분 후 2.2%를 보였다. 반응 가스인 CO 가스의 비율은 반응 시간 25분 후 1.7%를, 70분 후 0.6%를 보였다. 또한 생성 가스 중 CO2 가스의 비율은 반응 시간 25분 후 3.0%를, 70분 후 2.1%를 보였다. CO:H2O의 비율이 1:3인 경우 H2 가스의 비율은 반응 시간 10분 후 4.9%를, 70분 후 7.4%를 보였다. CO 가스의 비율은 반응 시간 10분 후 2.3%를, 70분 후 0.1%를 보였다. 또한 CO2 가스의 비율은 반응 시간 10분 후 2.4%를, 70분 후 1.9%를 보였다. CO:H2O의 비율이 1:4인 경우 H2 가스의 비율은 반응 시간 25분 후 8.3%를, 70분 후 8.4%를 보였다. CO 가스의 비율은 반응 시간 10분 후 0.4%를, 70분 후 1.8%를 보였다. 또한 CO2 가스의 비율은 반응 시간 10분 후 1.7%를, 70분 후 2.6%를 보였다.
400℃의 HTWGSR에서 CO:H2O의 비율이 1:2인 경우 생성 가스 중 H2 가스의 비율은 반응 시간 10분 후 4.8%를, 70분 후 2.6%를 보였다. 반응 가스인 CO 가스의 비율은 반응 시간 10분 후 4.0%를, 70분 후 1.9%를 보였다. 또한 생성 가스 중 CO2 가스의 비율은 반응 시간 10분 후 2.8%를, 70분 후 2.1%를 보였다. CO:H2O의 비율이 1:3인 경우 H2 가스의 비율은 반응 시간 25분 후 6.9%를, 70분 후 4.4%를 보였다. CO 가스의 비율은 반응 시간 25분 후 0.9%를, 70분 후 0.4%를 보였다. 또한 CO2 가스의 비율은 반응 시간 25분 후 2.3%를, 70분 후 2.3%를 보였다. CO:H2O의 비율이 1:4인 경우 H2 가스의 비율은 반응 시간 10분 후 5.3%를, 70분 후 9.0%를 보였다. CO 가스의 비율은 반응 시간 10분 후 2.0%를, 70분 후 0.2%를 보였다. 또한 CO2 가스의 비율은 반응 시간 10분 후 4.5%를, 70분 후 2.2%를 보였다.
반응이 시작되기 전의 총 가스 유량 대비 CO 가스의 비율은 CO:H2O=1:2의 경우 29.3%, CO:H2O=1:3의 경우 19.5%, CO:H2O=1:4의 경우 14.6%였다.
Fig. 5를 보면 알 수 있듯이 H2와 CO2 가스 생성과 CO 가스 비율의 감소는 반응 가스인 CO는 반응의 진행과 함께 감소하고 생성 가스인 H2와 CO2는 반응의 진행과 함께 생성되는 전형적인 WGS 반응을 보여주고 있다.
HTWGSR의 각 온도에서 CO:H2O의 비율 1:4에서 H2 가스 비율은 CO:H2O의 비율 1:2와 1:3인 경우와 비교하여 높은 값을 보였다. 이는 Fe/Cr 촉매 펠릿의 경우 H2 가스 발생량 측면에서는 CO:H2O의 비율은 1:4가 유리하다는 것을 의미한다.
Fig. 6은 제조한 Fe/Cr 촉매 펠릿을 이용한 HTWGSR의 각 온도에서 CO:H2O 비율에 따른 반응 시간과 CO 전환율과의 관계를 나타낸다.
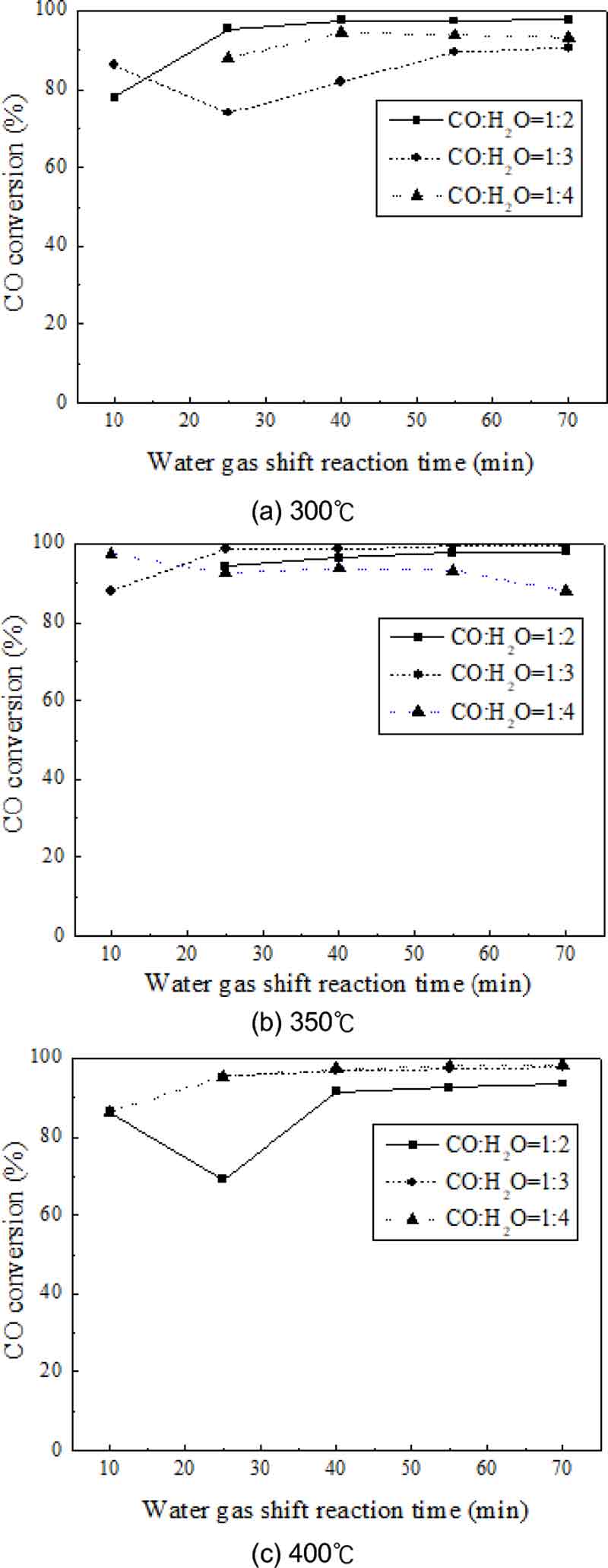
Relationship between reaction time and CO conversion for each CO:H2O ratio and temperature during HTWGSR using Fe/Cr catalyst pellet
300℃의 HTWGSR에서 CO:H2O의 비율이 1:2인 경우 CO 전환율은 반응 시간 10분 후 78.0%를 보였으며 시간 경과와 함께 증가하여 70분 후 97.6%를 보였다. CO:H2O의 비율이 1:3인 경우 CO 전환율은 반응 시간 10분 후 86.0%를 보였으며 25분 후 74.0%로 감소한 후 시간 경과와 함께 증가하여 70분 후 90.6%를 보였다. CO:H2O의 비율이 1:4인 경우 CO 전환율은 반응 시간 25분 후 88.0%를 보였으며 40분 후 94.0%로 증가한 후 시간이 지나도 거의 일정한 값을 유지하며 70분 후 93.2%를 보였다.
350℃의 HTWGSR에서 CO:H2O의 비율이 1:2인 경우 CO 전환율은 반응 시간 25분 후 94.0%를 보였으며 시간 경과와 함께 증가하여 70분 후 97.8%를 보였다. CO:H2O의 비율이 1:3인 경우 CO 전환율은 반응 시간 10분 후 88.0%를 보였으며 25분 후 98.6%로 증가한 후 시간이 지나도 거의 일정한 값을 유지하며 70분 후 99.3%를 보였다. CO:H2O의 비율이 1:4인 경우 CO 전환율은 반응 시간 10분 후 97.3%를 보였으며 25분 후 92.5%로 감소한 후 시간 경과와 함께 감소하여 70분 후 88.0%를 보였다.
400℃의 HTWGSR에서 CO:H2O의 비율이 1:2인 경우 CO 전환율은 반응 시간 10분 후 86.0%를 보였으며 25분 후 69.0%로 감소한 후 시간 경과와 함께 증가하여 70분 후 93.5%를 보였다. CO:H2O의 비율이 1:3인 경우 CO 전환율은 반응 시간 25분 후 95.5%를 보였으며 시간 경과와 함께 증가하여 70분 후 97.7%를 보였다. CO:H2O의 비율이 1:4인 경우 CO 전환율은 반응 시간 10분 후 86.4%를 보였으며 시간 경과와 함께 증가하여 70분 후 98.3%를 보였다.
300℃의 HTWGSR에서 CO 전환율은 CO:H2O의 비율이 1:2인 경우가 1:3, 1:4인 경우보다 반응 시간이 경과하면 높은 경향을 보였다. 350℃의 HTWGSR에서 CO 전환율은 CO:H2O의 비율이 1:3인 경우에서 1:2, 1:4인 경우보다 높은 경향을 보였으며 400℃의 HTWGSR에서 CO 전환율은 CO:H2O의 비율이 1:3, 1:4인 경우에서 1:2인 경우보다 높은 경향을 보였다.
Fig. 6을 보면 알 수 있듯이 300℃의 HTWGSR의 경우 CO:H2O의 비율이 1:2, 1:4인 경우에서, 350℃의 HTWGSR의 경우 CO:H2O의 비율이 1:2, 1:3인 경우에서, 400℃의 HTWGSR의 경우 CO:H2O의 비율이 1:3, 1:4인 경우에서 반응 시간 25분 후에 CO 전환율은 거의 일정한 값을 보였다. 또한 300℃의 HTWGSR의 경우 CO:H2O의 비율이 1:3일 때 반응 시간 25분 후에 CO 전환율이 증가하는 경향을, 350℃의 HTWGSR의 경우 CO:H2O의 비율이 1:4일 때 반응 시간 25분 후에 CO 전환율이 약간 감소하는 경향을, 400℃의 HTWGSR의 경우 CO:H2O의 비율이 1:2일 때 반응 시간 40분 후에 CO 전환율은 거의 일정한 경향을 보였다.
각 HTWGSR의 반응 온도에서 CO:H2O 비율에 따른 반응 시간과 CO 가스 전환율을 종합적으로 고려하였을 때 반응 시간은 약 40분 정도가 적합할 것으로 판단된다.
Fig. 7은 제조한 Fe/Cr 촉매 펠릿을 이용한 HTWGSR의 각 온도와 CO:H2O 비율 변화에 따른 평균 CO 전환율과의 관계를 나타낸다.
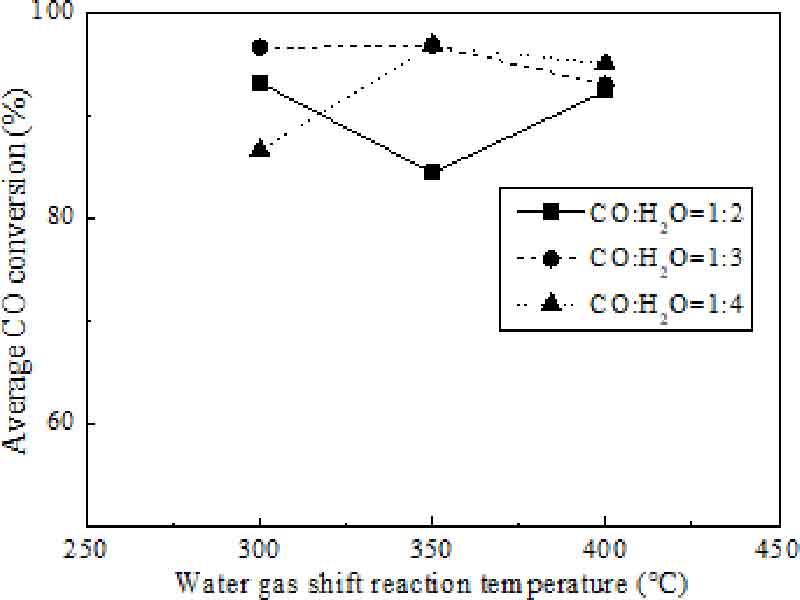
Relationship between reaction temperature and average CO conversion for each CO:H2O ratio in HTWGSR using Fe/Cr catalyst pellet
300℃의 HTWGSR에서 평균 CO 전환율은 CO:H2O의 비율이 1:3일 때 96.5%로 높은 값을 보였다. 350℃의 HTWGSR에서 평균 CO 전환율은 CO:H2O의 비율이 1:3일 때와 1:4일 때 96.7%로 높은 값을 보였다. 400℃의 HTWGSR에서 평균 CO 전환율은 CO:H2O의 비율이 1:4일 때 95.0%로 높은 값을 보였다.
Fig. 7을 보면 300℃와 350℃의 HTWGSR에서 높은 CO 전환율을 얻기 위해서는 CO:H2O 비율은 1:3이 가장 적합하며 400℃의 HTWGSR에서 CO:H2O 비율은 1:4가 가장 적합할 것으로 판단된다.
이상의 결과로부터 제조한 Fe/Cr 촉매 펠릿을 이용한 HTWGSR은 95.0%의 높은 CO 전환율에 도달할 수 있음을 확인할 수 있었다. 또한 CO 전환율 면에서 300℃와 350℃에서는 CO:H2O의 비율 1:3이, 400℃에서는 CO:H2O의 비율 1:4가 가장 적절하다는 것을 알 수 있었다. 그리고 향후 폐플라스틱 가스화에서 생성되는 CO, CO2, H2, CH4 가스 조성에서 제조한 Fe/Cr 촉매 펠릿의 HTWGSR 특성에 관한 연구가 필요할 것으로 판단된다.
4. 결 론
본 연구에서는 HTWGSR에 적용하고자 Fe/Cr 촉매 펠릿을 제조하였다. 촉매 펠릿은 공침법으로 제조한 Fe/Cr 촉매 분말을 압축 성형하여 제조하였다. Fe/Cr 촉매 펠릿을 이용한 HTWGSR은 300-400℃에서 CO:H2O의 비율을 1:2, 1:3, 1:4로 하여 진행하였으며 GHSV는 약 10,000 h-1이었다. 반응 온도와 CO:H2O 비율에 따른 CO 전환율을 평가하여 다음과 같은 결론을 얻었다.
- 1) XRD 분석 결과 제조한 Fe/Cr 촉매 분말은 F2O3- Cr2O3의 상을 보였다.
- 2) 제조한 Fe/Cr 촉매 펠릿은 EDXS 분석 결과로부터 Fe과 Cr을 함유하는 것을 확인할 수 있었으며 BET 분석 결과 5.88 m2/g의 표면적, 11.17 nm의 기공 직경, 0.026 mL/g의 기공 부피를 보였다.
- 3) HTWGSR의 각 온도에서 생성 가스 중 H2 가스 비율은 CO:H2O의 비율이 1:4인 경우가 1:2와 1:3인 경우와 비교하여 높은 값을 보였다.
- 4) HTWGSR의 각 온도에서 CO:H2O 비율에 따른 반응 시간과 CO 가스 전환율을 종합적으로 고려하였을 때 반응 시간은 약 40분 정도가 가장 적합할 것으로 판단하였다.
- 5) HTWGSR의 300℃에서 평균 CO 전환율은 CO:H2O의 비율이 1:3일 때 96.5%, 350℃에서 CO:H2O의 비율이 1:3, 1:4일 때 96.7%, 400℃에서 CO:H2O의 비율이 1:4일 때 95.0%로 높은 값을 보였다.
- 6) 제조한 Fe/Cr 촉매 펠릿을 이용한 HTWGSR은 95.0%의 높은 CO 전환율에 도달할 수 있음을 확인할 수 있었다.
- 7) HTWGSR의 CO 전환율을 고려하면 300℃와 350℃에서는 CO:H2O의 비율 1:3이, 400℃에서는 CO:H2O의 비율 1:4가 가장 적절하다는 것을 알 수 있었다.
Acknowledgments
본 연구는 환경부와 한국환경산업기술원의 “폐플라스틱 활용 원료・연료화 기술개발 사업(No. 2022003490001)”으로 추진된 것으로 환경부와 한국환경산업기술원의 재정 지원에 감사드립니다.
References
-
H. H. Shah, M. Amin, A. Iqbal, I. Nadeem, M. Kalin, A. M. Soomar, and A. M. Galal, “A review on gasification and pyrolysis of waste plastics”, Frontiers in Chemistry, Vol. 10, 2023, pp. 960894.
[https://doi.org/10.3389/fchem.2022.960894]

-
D. Saebea, P. Ruengrit, A. Arpornwichanop, and Y. Patcharavorachot, “Gasification of plastic waste for synthesis gas production”, Energy Reports, Vol. 6, Suppl. 1, 2020, pp. 202-207.
[https://doi.org/10.1016/j.egyr.2019.08.043]

-
C. J. Moore, “Synthetic polymers in the marine environment: a rapidly increasing, long-term threat”, Environmental Research, Vol. 108, No. 2, 2008, pp. 131-139.
[https://doi.org/10.1016/j.envres.2008.07.025]

-
F. D. B. de Sousa, “Management of plastic waste: a bibliometric mapping and analysis”, Waste Management & Research: The Journal for a Sustainable Circular Economy, Vol. 39, No. 5, 2021, pp. 664-678.
[https://doi.org/10.1177/0734242X21992422]

-
C. Wu and P. T. Williams, “Hydrogen production by steam gasification of polypropylene with various nickel catalysts”, Applied Catalysis B: Environmental, Vol. 87, No. 3-4, 2009, pp. 152-161.
[https://doi.org/10.1016/j.apcatb.2008.09.003]

-
M. He, B. Xiao, Z. Hu, S. Liu, X. Guo, and S. Luo, “Syngas production from catalytic gasification of waste polyethylene: influence of temperature on gas yield and composition”, International Journal of Hydrogen Energy, Vol. 34, No. 3, 2009, pp. 1342-1348.
[https://doi.org/10.1016/j.ijhydene.2008.12.023]

-
V. Wilk and H. Hofbauer, “Conversion of mixed plastic wastes in a dual fluidized bed steam gasifier”, Fuel, Vol. 107, 2013, pp. 787-799.
[https://doi.org/10.1016/j.fuel.2013.01.068]

-
G. Lopez, M. Artetxe, M. Amutio, J. Bilbao, and M. Olazar, “Thermochemical routes for the valorization of waste polyolefinic plastics to produce fuels and chemicals. A review”, Renewable and Sustainable Energy Reviews, Vol. 73, 2017, pp. 346-368.
[https://doi.org/10.1016/j.rser.2017.01.142]

-
E. Baraj, K. Ciahotný, and T. Hlinčík, “The water gas shift reaction: catalysts and reaction mechanism”, Fuel, Vol. 288, 2021, pp. 119817.
[https://doi.org/10.1016/j.fuel.2020.119817]

-
H. S. Na, D. W. Jeong, W. J. Jang, Y. L. Lee, and H. S. Roh, “A study on Cu based catalysts for water gas shift reaction to produce hydrogen from waste-derived synthesis gas”, Journal of Hydrogen and New Energy, Vol. 25, No. 3, 2014, pp. 227-233.
[https://doi.org/10.7316/KHNES.2014.25.3.227]

-
S. R. J. Byron, M. Loganathan, and M. S. Shantha, “A review of the water gas shift reaction kinetics”, International Journal of Chemical Reactor Engineering, Vol. 8, No. 1, 2010, pp. 1-34.
[https://doi.org/10.2202/1542-6580.2238]

-
J. M. Yun, Y. S. Choi, J. B. Kim, C. H. Ryu, and G. J. Hwang, “Water gas shift reaction using the commercial catalyst pellets from the gases by waste plastic gasification”, Journal of Hydrogen and New Energy, Vol. 34, No. 4, 2023, pp. 327-333.
[https://doi.org/10.7316/JHNE.2023.34.4.327]

-
F. Meshkani, M. Rezaei and M. Jafarbegloo, “Preparation of nanocrystalline Fe2O3-Cr2O3-CuO powder by a modified urea hydrolysis method: a highly active and stable catalyst for high temperature water gas shift reaction”, Materials Research Bulletin, Vol. 64, 2015, pp. 418-424.
[https://doi.org/10.1016/j.materresbull.2014.12.038]

-
D. B. Pal, R. Chand, S. N. Upadhyay, and P. K. Mishra, “Performance of water gas shift reaction catalysts: a review”, Renewable and Sustainable Energy Reviews, Vol. 93, 2018, pp. 549-565.
[https://doi.org/10.1016/j.rser.2018.05.003]

-
P. Ebrahimi, A. Kumar, and M. Khraisheh, “A review of recent advances in water-gas shift catalysis for hydrogen production”, Emergent Materials, Vol. 3, 2020, pp. 881-917.
[https://doi.org/10.1007/s42247-020-00116-y]

-
T. Moeini and F. Meshkani, “Facile synthesis of M-CuFe2O4 (M=Al2O3, CeO2, La2O3, ZrO2, Mn2O3) catalysts using a one-pot method and their applications in high-temperature water gas shift reaction”, International Journal of Hydrogen Energy, Vol. 48, No. 16, 2023, pp. 6370-6383.
[https://doi.org/10.1016/j.ijhydene.2022.07.045]

-
H. Qin, Y. He, P. Xu, D. Huang, Z. Wang, H. Wang, Z. Wang, Y. Zhao, Q. Tian, and C. Wang, “Spinel ferrites (MFe2O4): synthesis, improvement and catalytic application in environment and energy field”, Advances in Colloid and Interface Science, Vol. 294, 2021, pp. 102486.
[https://doi.org/10.1016/j.cis.2021.102486]

-
M. I. Ariëns, L. G. A. van de Water, A. I. Dugulan, E. Brück, and E. J. M. Hensen, “Substituting chromium in iron-based catalysts for the high-temperature water–gas shift reaction”, ACS Catalysis, Vol. 12, No. 22, 2022, pp. 13838-13852.
[https://doi.org/10.1021/acscatal.2c03871]

-
S. G. Lee, J. Kwak, and J. M. Sohn, “The study on the catalytic performance and characterization of La0.9Sr0.1Cr0.7B0.3O3±δ (B=Mn, Ni, Fe, Ru) for high temperature water-gas shift reaction with simuated coal-derived syngas”, Journal of Hydrogen and New Energy, Vol. 24, No. 6, 2013, pp. 543-549.
[https://doi.org/10.7316/KHNES.2013.24.6.543]

-
D. W. Jeong, A. Jha, W. J. Jang, W. B. Han, and H. S. Roh, “Performance of spinel ferrite catalysts integrated with mesoporous Al2O3 in the high temperature water-gas shift reaction”, Chemical Engineering Journal, Vol. 265, 2015, pp. 100-109.
[https://doi.org/10.1016/j.cej.2014.12.045]