수소연료전지 폐기물 기반 백금촉매 재자원화 시 침출 공정인자 연구
2024 The Korean Hydrogen and New Energy Society. All rights reserved.
Abstract
Platinum group metal (PGM) are important rare metals used in advanced industries, and their reserves are geographically concentrated, limiting their stable global supply. This study is an experimental study to derive process conditions that show the maximum and optimal leaching rate by appropriately combining three process factors: first, leaching concentration, second, leaching temperature, and third, concentration time, in the leaching process, which is the most important recycling process for platinum contained in trace amounts in various wastes such as first, waste catalyst (solid), second, waste catalyst (liquid), third, waste water, and fourth, waste membrane electrode assembly generated during the hydrogen fuel cell manufacturing process. As a result of a comparative leaching test of PGM with several oxidizing agents, aqua regia, which has a strong oxidizing power, was used as a platinum leaching agent because it generates nitrosyl chloride.
Keywords:
Hydrogen fuel cell, Leaching rate, Aqua regia, Waste catalyst, Concentration, Temperature키워드:
수소연료전지, 침출률, 왕수, 폐촉매, 농도, 온도1. 서 론
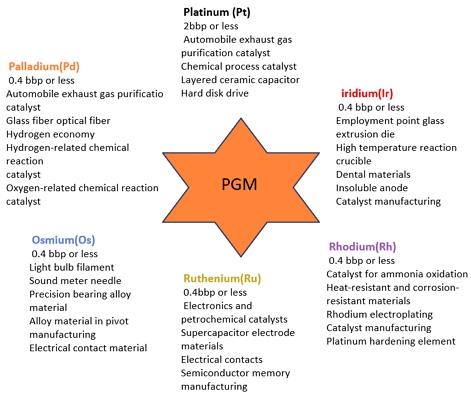
최근 전 세계적으로 자국의 주요 자원 보호, 환경 보전과 지속 가능한 개발에 대한 전 세계적인 관심이 증가하면서 국가는 자원 순환에 대한 투자를 확대하고 있다1). 이러한 글로벌 트렌드 속에서 수소에너지가 특히 주목받고 있는 이유는 그 환경적 이점과 함께 전통적 에너지원과 비교했을 때 높은 에너지 효율성과 광범위한 응용 가능성 때문이다2). 일부 주요 백금족 금속에 대해 수요와 공급의 불균형으로 가격이 폭등하는 사례가 발생하고 있으며 특히 우리나라의 희소금속 자원의 부재(자급률 1.5 % 수준)로 인한 수급 불균형과 가격 불안정을 잠재울 방법은 안전한 공급망 구축을 통한 기업 및 국가 경쟁력 확보가 전략적 대안이라고 판단된다. 희소금속 자원의 부재는 첨단 산업 분야에 점점 더 큰 부담으로 작용하고 있으며 그중 백금족 금속(platium group metals)은 주기율표 8족에 속하는 6종류의 금속으로 백금(Pt), 로듐(Rh), 루테늄(Ru)과 팔라듐(Pd), 이리듐(Ir), 오스뮴(Os)의 6개 금속이 해당한다. 이 금속들은 밀도에 따라 백금, 이리듐, 오스뮴 등은 중백금족(밀도 약 22 g/cm3)으로, 팔라듐, 로듐, 루테늄 등은 경백금족(밀도 약 12 g/cm3)으로 구분된다3,4). 또한 이들 금속이 지구 지표면인 지각에 존재하는 양을 분석한 결과 아주 미량으로 백금의 경우 2 ppb 이하, 팔라듐은 0.4 ppb 이하, 로듐은 0.4 ppb 이하, 오스뮴은 0.4 ppb 이하, 이리듐은 0.4 ppb 이하, 루테늄은 0.4 ppb 이하로 매우 희소하며 각 금속을 활용하는 각 산업 분야는 Fig. 1과 같이 다양하다. 따라서 백금족 금속은 최첨단 산업 분야의 특수한 기능을 부여하는 중요한 핵심 금속으로 활용 분야가 매우 넓고 다양하다고 할 수 있다.
산업적으로 중요한 소재 원료인 백금족 금속은 희귀하며 세계 몇몇 나라의 일부 지역에 편중되어 있다. 백금족 금속의 주요 자원 보유국 및 생산국은 남아프리카공화국, 러시아, 캐나다, 미국, 짐바브웨, 콜롬비아, 보츠와나, 호주 등이며 이들 중 남아프리카공화국과 러시아가 전체 생산량의 80-90%를 점유하고 있다.
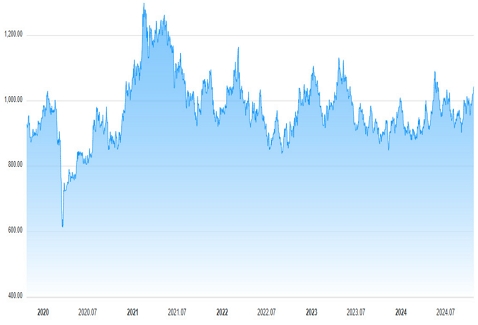
이와 같은 백금족 금속 부존 자원의 희소성 및 편재성은 백금족 금속의 안정적 공급의 불안정성을 가중시키고 있다. 따라서 선진 산업 국가들은 백금족 금속의 안정적 확보를 위하여 치열한 경쟁을 벌이고 있으며 재생 백금도 고순도(3N5급, 순도 99.95%; 불순물 함유량 500 ppm 이하)가 확보되면 국제 시세 대비 신품 동일 가격의 97% 이상으로 거래되고 있다. 최근 5년간의 국제 백금 가격 차트(Fig. 2)를 분석하면 2020년 3월 최저점 USD 620/T.oz에서 2021년 2월 최고점 USD 1,300/T.oz로 가격이 210% 상승한 뒤 유지되다가 이후 2024년 10월 현재 USD 950-1,050/T.oz로 2020년 대비 160% 인상된 가격으로 계속 유지되고 있는 실정이다5).
따라서 선진 산업 국가들은 백금족 금속의 안정적 확보를 위하여 치열한 경쟁을 벌이고 있으며 폐전자 부품 스크랩, 폐액과 폐촉매 등의 폐자원으로부터 회수 및 정련하는 백금족 금속의 자원 순환 재활용 기술 개발에 많은 투자를 하고 있다. 그러나 백금족 금속에 관한 회수화 기술, 정련화 기술, 고순도화 기술은 남아프리카공화국, 러시아와 같은 광물 자원 보유국을 비롯하여 영국, 독일, 일본, 미국 등 몇몇 선진국의 제조업체를 중심으로 발달한 관계로 각국의 백금족 금속의 생산을 위한 중요 기술인 침출(용해) 기술, 정련 기술 및 환원 기술 역시 소수의 기업에 독점적으로 집중되어 있다. 특히 다른 금속에 비하여 가격이 굉장히 고가인 백금족 금속은 부가가치가 매우 높기 때문에 기술 보유국들은 관련 기술 이전을 상당히 꺼리고 있으며 그 기술 노하우를 철저한 보안을 통해 기밀로 유지하고 있다. 수소 경제(hydrogen economy) 시대는 석유 대신 수소가 주 에너지로 사용되는 그린 에너지 시대(green energy generation)를 의미한다. 각 나라 수소 경제 마스터플랜(master plan)을 작성하여 석유, 석탄, 천연가스, 신재생에너지 등을 이용하여 수소를 생산하고 연료전지를 통해 수소를 활용하는 경제사회를 수소 경제라 지칭하고 있으며 기존의 탄소 경제와 수소 경제를 네 가지 측면에서 비교하면 Table 1과 같다.
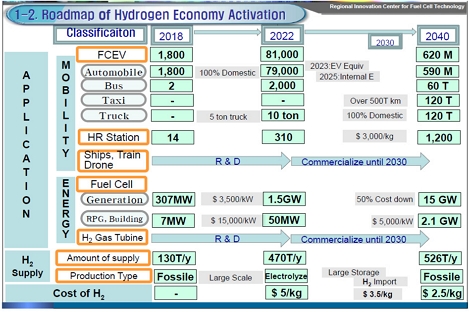
국내 수소 경제 활성화 전망을 보면 기존 산업 및 연료전지 수요 증대 등을 기반으로 수소 경제 시대가 점차 더 가시화되고 있다. Fig. 3의 수소 경제 활성화 로드맵을 참조하면 2022년에는 수소연료전지 자동차(fuel cell vehicle, FCV)가 81,000대, 수소 충전소는 310개소로 전국적으로 충전소가 설치되어 인프라가 더 조밀하게 구축되고 있으며 예상되는 수소연료전지 전기 발전량은 1.5 GW이다. 수소차의 시장 확대를 위해서는 연료전지 내구성 문제와 연료전지 가격 등을 해결하여야 한다6). 수소 제조 원가 역시 기술 개발과 제조 공정 개선으로 2030년에는 $2.5/kg (H2)으로 낮아질 전망이다. 현재 FCV 분야에 소요되는 백금량을 산출해 보면 전 세계에서 가장 많이 판매되는 현대 NEXO (Hyundai Motors, Seoul, Korea) 1대당 백금촉매 약 40 g이 소요된다. 이를 2022년의 81,000대 기준으로 계산해 보면 자동차 분야에만 백금 소요량은 무려 3,240 kg이다.
백금의 물리적, 화학적 특징 및 용도를 보면 최대 용도는 촉매이다(Table 2).
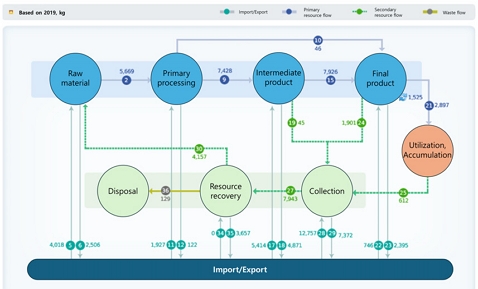
한국생산기술연구원 자원순환기술지원센터의 국가통합자원관리시스템(Korean National Material Flow Analysis, K-MFA)에서 2019년 조사한 백금 수출입 간이 흐름도(Fig. 4)를 참조하면 국내 전 산업 분야에서의 백금 총 수요량(최종 제품 함유) 예상량이 8,551 kg인데 FCV 분야에만 사용되는 백금량이 3,240 kg으로 전체 수요량의 약 38%를 점유하고 있는 상황이다. 또한 백금은 절대적으로 부족한 상태이며 폐자원으로부터 백금의 재자원화, 원료화하는 재사용 비율도 총 발생량 7,943 kg에서 4,157 kg으로 발생량의 절반 정도인 52% 정도의 회수 정련화 비율의 기술 수준에 머무르고 있으며 나머지 48%는 재자원화를 위하여 해외로 반출하고 있는 형편이다. 백금 촉매가 있는 고분자 연료전지 스텍(stack)의 수명이 승용차의 경우 8,000시간 이상, 상용차의 경우 30,000시간 이상 확보해야 한다7).
국내 백금 재활용의 경우 강산화제에 용해되기 때문에 회수할 수 있으나 회수율이 선진국인 일본과 영국 대비 현저하게 낮으며 백금족 금속에 대한 회수 및 정제, 고순화 공정 기술은 자국의 원천 기술로 철저히 보호하고 있어 백금족 금속에 대한 대한민국의 자체적인 회수, 정제, 정련 기술 연구 개발이 시급하다고 사료된다4,8).
따라서 본 연구에서는 백금족 금속을 몇 가지 산화제로 침출(용해) 비교 테스트(Table 3)한 데이터를 참조하여 강력한 산화력을 가진 왕수(aqua regia) 사용 시 염화나이트로실(nitrosyl chloride, NOCl)이 생성되므로 백금 침출제로 사용하기로 하였다.
2. 실 험
2.1 시료 선정 및 실험 준비
폐수소연료전지 기반 폐기물 종류를 보면 폐촉매(고상), 폐촉매(액상), 폐기물(고상, 보루), 폐 membrane electrode assembly (MEA) 4종류이다. 백금의 회수 및 정련을 위한 일반적인 표준 공정은 전처리(pre-treatment)로 폐기물 형태와 형상에 따라 물리적 분리 및 분쇄, 파쇄 후 회화 공정(carcination)을 시작으로 용해 공정, 농축 공정, 여과 및 수세 공정, 반응 공정, 여과 및 수세 공정, 환원 공정, 여과 및 수세 공정 후 후처리(post-treatment) 공정, 건조(drying) 및 ingot이다.
실험 준비와 시료 샘플링은 Table 4에 제시된 방법으로 단계별로 실시하였다.
침출 용액인 왕수는 각 시료마다 500 mL씩 건욕(make-up)하여 사용한다. 왕수는 다음 반응에 의하여 건욕된다.
| (1) |
이때 HCl:HNO3는 3:1 몰수비 혼합이 정확하지만 진한 염산과 진한 질산을 3:1 부피비(375:125 mL)로 혼합하여 사용한다.
실험 계획(Table 5)에 기반하여 침출 용액인 왕수 농도 변수 4개(10, 20, 30, 40 wt%), 농축 온도 변수 5개(50, 60, 70, 80, 90, 100℃), 농축 시간 변수 3개(1, 2, 3시간)별로 각각 시료를 10 g씩 준비한다. 그리고 2,000 mL의 이중 자켓 중탕형 반응조에 먼저 건욕해 둔 침출 용액인 왕수를 500 mL 계량하여 넣고 그다음 채취한 시료 10 g씩을 순차적으로 넣고 실험을 수행하였다. 그리고 각각 10 mL씩 채취하여 원자흡광광학분석기(atomic absorption spectrometer, AAS)를 이용하여 분석하였다.
각각의 최종 침출액을 여과지로 여과 후 시료 채취하여 AAS를 통해 산출된 백금 농도 분석 결과치(ppm)에 침출액 양을 곱한 후 모재량(10 g)을 나누고 단위 환산을 위하여 1,000을 나누면 각각의 조건에서 침출된 백금량(g/kg)을 계산할 수 있다. 이를 통해 각각의 조건에서 나온 침출률(침출 후 백금 함량과 침출 전 백금 함량 비율, %) 계산값을 비교 평가하였다.
3. 결과 및 고찰
본 연구에서는 침출 용액으로 왕수를 사용하였다. 일차적으로 농도에 따른 침출률을 비교하여 침출 용액의 최적 조건을 설정한 후 그 조건을 고정하고 이차적으로 농축 온도와 침출 시간을 변화시켜 실험을 진행하였다. 그리고 침출 시간에 따른 침출률 변화 추이를 통해 각 조건마다 침출되는 속도를 판단하고자 하였다.
3.1 왕수 농도별 침출률 변화 실험 평가
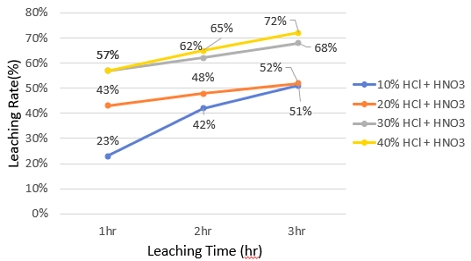
왕수 10, 20, 30, 40 wt% 농도로 농축 온도 60℃, 교반기 400 RPM 속도 조건에서 백금 침출 실험을 수행하였을 때 농도 40 wt%에서 침출 시간 3시간이 경과하였을 때 84%의 침출률이 산출되어 최대 침출률이 도출되었다(Fig. 5).
3.2 농축 온도 변화에 따른 침출률 변화 실험 평가
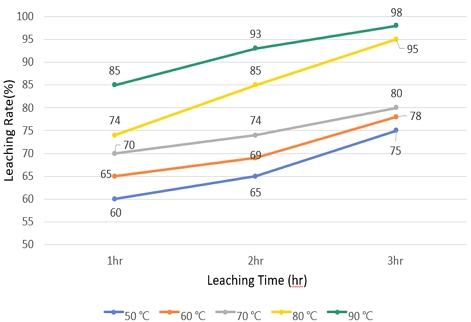
침출 용액에서 가장 높은 침출률을 보였던 40 wt% 왕수 조건에서 각각 50, 60, 70, 80, 90℃ 온도로 변화시켜 백금 침출률을 비교 평가하였다. Fig. 6을 참조하면 농축 3시간 경과 시 농축 온도 80℃에서 침출률 98%, 농축 온도 90℃에서 침출률 95%로 온도가 증가할수록 백금의 침출률이 증가하다가 농축 온도 90℃에서 침출률이 95%로 백금의 침출률이 감소하였다. 따라서 침출 시간 3시간 기준으로 침출하였을 때 농축 온도 80℃에서 98%의 침출률을 나타내어 최대 침출률이 도출되었다.
3.3 왕수 농도 40 wt% 기준 침출 시간에 따른 침출률 실험 평가
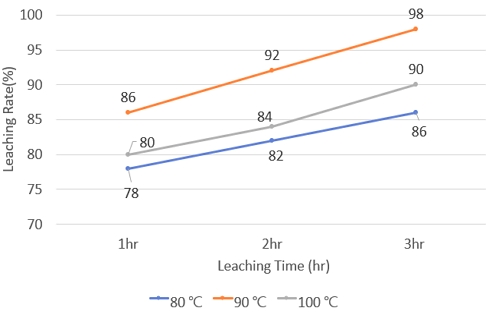
왕수 농도 40 wt%의 조건에서 농축 온도 80, 90, 100℃, 농축 시간 1, 2, 3시간의 침출 시간 변화에 따른 침출률 변화는 Fig. 7을 보면 농축 온도 90℃일 때 침출률 98%로 가장 높은 결과가 도출되었다.
4. 결 론
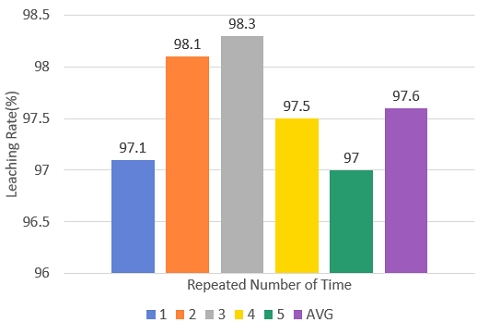
폐수소연료전지 기반 폐촉매(고상), 폐촉매(액상), 폐기물(고상, 보루), 폐 MEA의 4종류 폐기물에 함유된 백금의 최대 침출(용해) 공정 조건을 도출하는 데 있어 금 또는 백금족 금속을 용해하는 기본 화학물질인 왕수를 침출 용액으로 선정하였다. 실험 1단계는 왕수 농도별 침출률 변화를 실험 평가하였고 농도 40 wt% 조건에서 침출 시간 3시간이 경과하였을 때 84%의 침출률이 산출되어 최대 침출률이 도출되었다. 실험 2단계는 농축 온도 변화에 따른 침출률 변화를 실험 평가하였고 침출 시간 3시간 기준으로 침출하였을 때 농축 온도 80℃에서 98%의 침출률이 산출되어 최대 침출률이 도출되었다. 실험 3단계는 왕수 농도 40 wt% 기준 침출 시간에 따른 침출률을 실험 평가한 결과 농축 온도 90℃일 때 침출률이 98%로 가장 높은 결과가 도출되었다. 실험 1, 2, 3단계를 조합한 최대 침출률을 보이는 최적의 공정 조건은 왕수 농도 40 wt%, 농축 온도 90℃, 침출 시간 3시간일 때 최대 침출률 98%가 도출되었다. 이 최대 침출률을 보이는 최적의 공정 조건에서 반복 5회 재현성 실험한 결과 침출률 최소 97.0%, 최대 98.3%, 평균 97.6%로 도출되었다. 본 연구에서는 백금 자원 재순환을 위한 1단계인 폐자원 기반 최적 백금 침출률 공정 조건을 도출하였지만 2단계인 침출 회수된 백금에 함유된 각종 불순물(impurities)을 제거하여 고순도화하는 세부적인 정제, 정련 공정 조건 설계 및 각 공정별 유해 화학 물질 사용량 및 배출량을 최소화하는 친환경 공정 연구 개발과 수소 생산을 위한 다양한 수전해 기술 중 고분자 전해질 수전해에서 촉매로 사용되는 이리듐(Ir)의 침출 기술 확보도 추가적으로 필요하다고 사료된다9,10).
Acknowledgments
이 논문은 정부(환경부)의 재원으로 한국환경산업기술원의 지원을 받아 수행된 연구(지식기반환경서비스 특성화대학원사업)임.
References
-
C. Kim, G. Kim, and H. Kim, “Analysis of domestic and foreign policy and technology trends for hydrogen industry development”, Journal of Hydrogen and New Energy, Vol. 34, No. 2, 2023, pp. 122-131.
[https://doi.org/10.7316/JHNE.2023.34.2.122]

-
J. E. Shin, “Hydrogen policy trends and current status of hydrogen technology development by value chain”, Journal of Hydrogen and New Energy, Vol. 34, No. 6, 2023, pp. 562-574.
[https://doi.org/10.7316/JHNE.2023.34.6.562]

- B. C. Kim, S. Chae, J. Kim, and K. Yoo, “Oversea production status of gold, silver, platinum and palladium from scrap”, Journal of the Korean Institute of Resources Recycling, Vol. 27, No. 6, 2018, pp. 76-83.
- H. Lee, M. Lee, H. Joo, and G. Kim, “Study on institutional and technical supporting plans to activate resource recirculation of rare metals of waste metal resources”, Korea Environmental Policy Evaluation Institute, Seoul, 2011, pp. 1-164.
-
Johnson Matthey, “PGM market report: Feb 2021”, Focus on Catalysts, Vol. 2021, No. 4, 2021, pp. 2.
[https://doi.org/10.1016/j.focat.2021.03.006]

- W. Y. Lee, M. Kim, H. Oh, Y. J. Sohn, and S. G. Kim, “A review on prognostics of polymer electrolyte fuel cells”, Journal of Hydrogen and New Energy, Vol. 29, No. 4, 2018, pp. 339-356.
- Hydrogen and Fuel Cell Technologies Office, “Hydrogen and fuel cell technologies office multi-year program plan”, U. S. Department of Energy, 2024. Retrieved from https://www.energy.gov/eere/fuelcells/hydrogen-and-fuel-cell-technologies-office-multi-year-program-plan, .
-
L. J. Kim, H. Shin, and H. Y. Kang, “Investigation and analysis for the status of urban mining industry in Korea”, Journal of the Korean Institute of Resources Recycling, Vol. 25, No. 5, 2016, pp. 3-13.
[https://doi.org/10.7844/kirr.2016.25.5.3]

-
L. A. King, M. A. Hubert, C. Capuano, J. Manco, N. Danilovic, E. Valle, T. R. Hellstern, K. Ayers, and T. F. Jaramillo, “A non-precious metal hydrogen catalyst in a commercial polymer electrolyte membrane electrolyser”, Nature Nanotechnology, Vol. 14, 2019, pp. 1071-1074.
[https://doi.org/10.1038/s41565-019-0550-7]

-
A. A. H. Tajuddin, G. Elumalai, Z. Xi, K. Hu, S. Jeong, K. Nagasawa, J. Fujita, Y. Sone, and Y. Ito, “Corrosion-resistant non-noble metal electrodes for PEM-type water electrolyzer”, International Journal of Hydrogen Energy, Vol. 46, No. 78, 2021, pp. 38603-38611.
[https://doi.org/10.1016/j.ijhydene.2021.09.116]