심냉 증류를 통한 전자급 고순도 이산화탄소의 분리 공정에 대한 전산 모사 연구
2023 The Korean Hydrogen and New Energy Society. All rights reserved.
Abstract
In this study, a computer simulation work has been performed for the separation of electronic grade highly pure carbon dioxide more than 7 N purity through a cryogenic distillation process. For the cold utility as a cooling medium for a condenser of the cryogenic distillation column, propylene was utilized as a refrigerant in the vapor-recompression refrigeration cycle. Through this work, it was concluded that the cryogenic distillation column with two stage compression and refrigeration cycle were essential to obtain a highly-pure liquefied CO2.
Keywords:
Cryogenic distillation, Electronic grade, highly pure carbon dioxide, Separation process, Computer simulation, Thermodynamic model키워드:
심냉 증류, 전자급 고순도 이산화탄소, 분리 공정, 전산 모사, 열역학 모델1. 서 론
이산화탄소를 고순도로 정제하게 되면 공업용, 농업용, 의료용, 식품용 그리고 전자급 등의 용도로 사용할 수 있다1,2). Table 1에는 고순도 이산화탄소의 용도별 순도를 정리하여 나타내었다. 발전소의 연소 배기가스로 배출되는, 이산화탄소를 포함하고 있는 기상류를 습식 용매 또는 건식법을 이용한 이산화탄소 포집 공정 또는 분리막 공정을 거치면 어느 정도 농축된 이산화탄소를 얻을 수 있다3-6). Table 2에는 습식법, 건식법 및 분리막 공정에서 얻어지는 기상류의 조성을 각각 나타내었다. 각각의 공정을 거쳐 농축된 이산화탄소를 중간에 냉각기를 거치는 이단 압축 공정에 의해서 20 bar까지 가압시킨 후에 냉매를 이용한 증기 재압축 냉동 사이클을 통해서 액화시키거나 liquified natural gas 냉열을 활용하여 액화시키거나 발전사나 블루수소를 생산하는 공정 등에 적용하기 위한 연구가 매우 활발하고 진행되고 있다7,8). 본 연구에서는 가압하고 난 후 심냉 증류 공정을 거치고 나서 전자급 이상의 고순도 이산화탄소를 분리 및 정제하는 공정에 대한 전산 모사와 공정 최적화를 수행하였다. 심냉 증류탑에서 재비기에 대한 열원으로는 원료와의 열교환을 활용하였으며, 응축기에 필요한 유틸리티는 냉매를 이용한 냉동 사이클을 사용하였다. Fig. 1에는 고순도 액화 이산화탄소를 얻기 위한 이단 압축 공정, 심냉 증류 공정 및 증류탑의 응축기를 위한 프로필렌 냉동 사이클을 포함한 전체 공정에 대한 PRO/II 플로시트를 나타내었다.
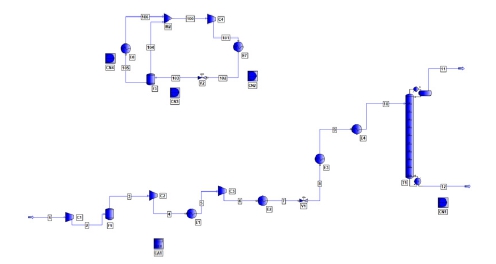
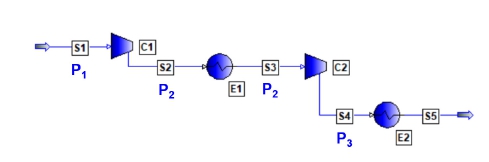
Schematic diagram for an overall process to obtain highly pure liquefied CO2 through a cryogenic distillation process with two-stage compression and vapor-recompression refrigeration cycle
Fig. 2에는 상압 근처의 이산화탄소를 포함하는 기상류를 20 bar까지 가압하기 위한 중간에 냉각기를 가지는 이단 압축 공정에 대한 PRO/II 플로시트를 나타내었다.
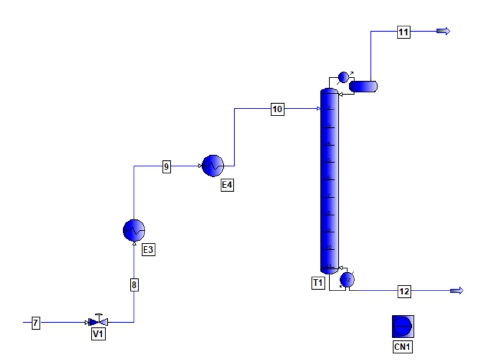
Fig. 3에는 이단 압축 공정을 거친 후, 심냉 증류 공정을 이용하여 증류탑 하부 제품으로 고순도 이산화탄소를 분리하는 공정에 대한 PRO/II 플로시트를 나타내었다.
Fig. 3에 의하면 질소 등이 포함된 이산화탄소 원료 가스가 E3에서 재비기에 필요한 열원을 공급하며, E4에서는 프로필렌 냉매에 의해서 더욱 냉각된 후 심냉 증류탑 상부로 주입된다. E3는 심냉 증류탑의 재비기의 heat duty와 동일하게 설정하였다. 이것은 원료 가스에 포함되어 있는 열원을 재비기에서 사용하는 것을 의미한다. 여기에서 질소 가스 등은 상부 기상류로 제거되고, 하부 액상류에는 전자급 고순도 이산화탄소가 분리되어 포집된다. 원료 대비 이산화탄소의 회수율은 79.5% 이상으로 설정하였다.
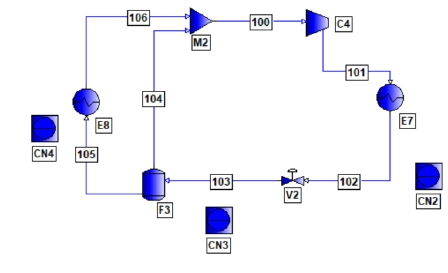
Fig. 4에는 프로필렌 냉매를 이용한 증기 재압축 냉동 사이클에 대해서 PRO/II를 사용한 플로시트를 나타내었다. Fig. 4에 의하면 대기압보다 약간 높은 압력 조건에서 이슬점 상태에 있는 냉매는 압축기에 의해 충분히 높은 압력까지 가압된 후에 냉매 응축기에 의해서 45℃까지 냉각된다. 이때, 냉각된 냉매는 응축기 후단에서 액화가 일어나는 압력까지 가압된다. 냉매 압축기 후단의 압력은 주어진 냉매의 45℃에서의 기포점 압력과 같다. 응축된 냉매는 줄-톰슨 팽창 밸브에 의해서 대기압보다 약간 높은 압력까지 팽창된다. 팽창이 일어난 후에는 증발도 같이 일어나게 되는데 증발하면서 잠열을 가져가므로 냉매의 온도는 급격히 떨어지게 된다. 이때 얻어지는 온도가 바로 주어진 냉매의 공급 온도가 된다. 팽창 밸브 후단에서 기상류는 냉매 온도는 낮지만, 열량이 없기 때문에 압축기 전단으로 보내지고, 액상류는 냉매 증발기로 주입된다. 그리고 후단에서는 포화 증기 상태에서 다시 압축기로 보내져 하나의 냉동 사이클을 이루게 된다.
2. 열역학 모델식
2.1 올바른 열역학 모델식의 선정
주어진 화학 공정의 전산 모사를 수행할 적에 고려해야 할 필수 불가결한 요소는 바로 올바른 열역학 모델식을 선정하는 것이다9). 본 연구에서는 SRK 모델식이 아닌, 삼차형 상태방정식 모델식 중에서 Peng-Robinson 상태방정식 모델식을 사용하였으며, 식 (1)에는 그 표현식을 나타내었다10).
| (1) |
식 (1)에서 ɑ와 b는 각각 에너지 매개변수와 크기 매개변수이며 이는 다음의 식 (2)와 식 (3)에 나타내었다.
| (2) |
| (3) |
2.2 새로운 alpha function의 선택
SRK 상태방정식에서 Pitzer가 최초로 제안한 이심인자의 함수로 표현한 alpha function은 환산온도가 증가하면 다시 증가하는 함수이므로 기본적으로 틀렸다11). 그래서 본 연구에서는 Twu 등11)이 제안한 새로운 alpha function을 사용하였으며, 그 표현식은 다음의 식 (4)와 같이 나타낼 수 있다.
| (4) |
식 (4)에서 Tr은 순수 성분의 환산온도이며, C1, C2및 C3 성분마다 다르게 지정된 순수 성분의 온도에 따른 증기압을 잘 추산하기 위한 매개변수들이다. Table 3에는 본 연구에서 사용한 성분들에 대한 Twu모델식의 계수들을 나타내었다.
3. 전산 모사
3.2 이산화탄소 압축 공정의 최적화
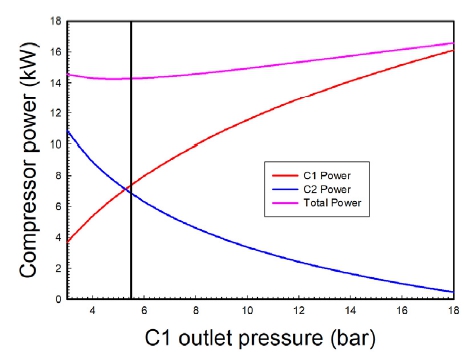
Fig. 5에는 첫 번째 압축기 후단의 압력의 함수로 첫 번째와 두 번째 압축기 소요 동력 및 총 소요 동력의 변화를 그래프로 도시하였다. Fig. 5에 의하면 첫 번째 압축기 후단의 압력이 증가하면 첫 번째 압축기의 소요 동력은 그에 비례해서 증가하고, 두 번째 압축기의 소요 동력은 감소하는 것을 알 수 있다. 한편 첫 번째 압축기와 두 번째 압축기 소요 동력의 총합은 첫 번째 압축기 후단 압력 5.477 bar에서 14.2781 kW로 최소가 되는 것을 알 수 있다. 즉 총 소요 동력의 합을 최소화시켜주는 최적의 중간 압력은 P1과 P3의 기하평균임을 알 수 있다. 이를 식으로 나타내면 식 (7)과 같다.
| (7) |
다음의 Table 6에는 이단 압축 공정에 대한 최적 조건에서의 전산 모사 결과를 요약하여 나타내었다.
3.3 심냉 증류 공정의 전산 모사
CO₂ 심냉 증류탑의 운전 압력은 19 bar이며, 이론 단수는 상부 응축기와 하부 재비기를 포함하여 12단으로 정하였다. 상부 기상류로 불순물을 제거하기 때문에 부분 응축기를 사용하였다. Table 7에는 심냉 증류탑에 대한 전산 모사 결과를 요약하여 정리하였다. Table 7을 보면 하부에서 N2, O2 및 CO 불순물의 합은 trace로 존재하며, 이산화탄소 순도는 거의 100%가 됨을 알 수 있다.
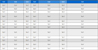
Simulation results summary for a cryogenic distillation column for the separation of highly pure CO₂
Fig. 6에는 심냉 증류탑 하부에서 원료 대비 이산화탄소 회수율 변화에 따른 상부 응축기의 heat duty와 환류 드럼의 온도 변화를 그래프로 도시하였다. Fig. 6에 의하면 심냉 증류탑 하부에서 이산화탄소 회수율이 증가할수록 심냉 증류탑에서 응축기의 heat duty는 감소하는 것을 알 수 있다. 이는 심냉 증류탑 하부에서 이산화탄소 회수율이 증가할수록 탑상 제품으로 얻어지는 기상류의 질량 유량이 줄어들기 때문이다. 따라서 1로 고정된 환류비에서는 당연히 응축기의 heat duty가 줄어들게 된다. 또한 심냉 증류탑 하부에서 이산화탄소 회수율이 증가할수록 환류 드럼의 온도 역시 낮아지는 경향을 보이고 있는데, 이는 비교적 고비점의 이산화탄소가 하부로 얻어질수록 상부 기상류에서는 이산화탄소의 몰분율이 감소하게 되어 이슬점 온도가 낮아지기 때문이다. 이로부터 유추해 보면 –45℃로 공급되는 프로필렌 냉매를 이용한 냉동 사이클을 이용할 경우 하부에서 이산화탄소의 회수율은 어느 정도 제한 조건이 있음을 알 수 있다. 즉 이산화탄소의 회수율을 너무 높여서 환류 드럼의 온도가 –45℃ 이하가 되면 안 된다.
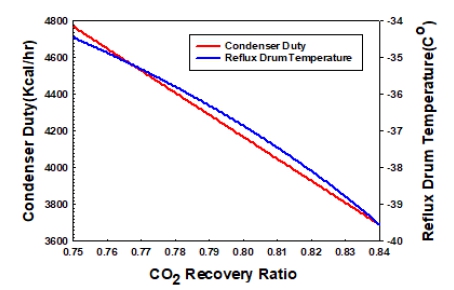
Plot of condenser duty and reflux drum temperature as a function of CO2 recovery ratio at a cryogenic distillation column bottom product
한편 Table 8에는 Table 2의 원료 가스를 기준으로 해서 이단 압축 후에 프로필렌 냉매를 이용해서 –40℃까지 온도를 낮추었을 경우에 얻어지는 액화 이산화탄소의 액화율과 조성을 나타내었다. Table 8에 의하면 습식법에 의해서 이산화탄소를 포집한 경우에는 수분을 제외하면 100% 순수한 이산화탄소를 액화시키기 때문에 액화율이 100%이고, 액화 이산화탄소의 농도도 100%가 된다. 그리고 건식법에 의한 이산화탄소 포집 공정은 액화율은 100%를 얻을 수 있지만, 순도는 99%로 비교적 낮으며 분리막 공정의 경우에는 액화율이 91%로 매우 낮으며 순도 또한 97.6%로 매우 낮다. 따라서 고순도의 전자급 이산화탄소를 얻기 위해서는 심냉 증류 공정이 필수적이라고 할 수 있다.
4. 결 론
증기 재압축 냉동 사이클을 이용한 심냉 증류를 통한 고순도 이산화탄소를 얻기 위한 전산 모사 결과 다음과 같은 결론을 얻을 수 있었다.
1) 단순히 기체 압축 후에 냉동 사이클을 통한 액화 공정만 활용할 경우 습식법을 이용한 이산화탄소 포집 공정을 제외하고 건식법 및 분리막을 이용한 포집 방법으로 7 N 이상의 고순도 이산화탄소를 얻으려면 냉동 온도가 –40℃보다 더 낮아지고 회수율이 더 떨어져야 함을 알 수 있었다.
2) 심냉 증류 공정을 이용하면 심냉 증류탑 하부에서 불순물 성분들인 N2, O2 및 CO의 조성의 합이 1.0086×10-8으로 거의 순수한 액체 이산화탄소를 얻을 수 있음을 알 수 있었다.
3) 중간에 냉각기를 거치는 이단 압축 공정에서 총 소요 동력을 최소화시켜 주는 최적의 중간 압력은 최초 압력과 최종 압력의 기하평균임을 알 수 있었다.
4) 심냉 증류탑 하부에서 이산화탄소 회수율이 증가할수록 심냉 증류탑 상부 기상류에서 비점이 낮은 성분들의 상대적인 조성이 증가하므로 환류 드럼의 온도가 낮아지는 것을 알 수 있었다. 또한 더욱 낮은 온도의 냉매를 사용해야 하므로 냉매 압축기의 소요 동력은 이에 비례해서 증가하는 것을 알 수 있었다.
Acknowledgments
본 연구는 2023년도 정부(과학기술정보통신부)의 재원으로 한국연구재단-CCU3050 사업의 지원을 받아 수행된 연구임(No.2022M3J2A1063788).
References
-
S. Valluri, V. Claremboux, and S. Kawatra, "Opportunities and challenges in CO2 utilization", Journal of Environmental Sciences, Vol. 113, 2022, pp. 322-344.
[https://doi.org/10.1016/j.jes.2021.05.043]

-
Q. Zhu, "Developments on CO2-utilization technologies" , Clean Energy, Vol. 3, No. 2, 2019, pp. 85-100.
[https://doi.org/10.1093/ce/zkz008]

-
Y. Le Moullec, T. Neveux, K. Makhloufi, D. Roizard, M. Kanniche, and E. Favre, "Development of a CO2 capture proc ess based on ammonia solvent and a dedicated composite hollow fibre membrane contactor", Energy Procedia, Vol. 63, 2014, pp. 651-658.
[https://doi.org/10.1016/j.egypro.2014.11.072]

-
R. Bouma, F. Vercauteren, P. van Os, E. Goetheer, D. Berstad, and R. Anantharaman, "Membrane-assisted CO2 liquefaction: performance modelling of CO2 capture from flue gas in cement production", Energy Procedia, Vol. 114, 2017, pp. 72-80.
[https://doi.org/10.1016/j.egypro.2017.03.1149]

-
Z. Rui, J. B. James, A. Kasik, and Y. S. Lin, "Metal-organic framework membrane process for high purity CO2 production", AIChE Journal, Vol. 62, No. 11, 2016, pp. 3836-3841.
[https://doi.org/10.1002/aic.15367]

-
J. C. L. Y. Fong, C. J. Anderson, G. Xiao, P. A. Webley, and A. F. A. Hoadley, "Multi-objective optimisation of a hybrid vacuum swing adsorption and low-temperature post-combustion CO2 capture", Journal of Cleaner Production, Vol. 111, Pt. A, 2016, pp. 193-203.
[https://doi.org/10.1016/j.jclepro.2015.08.033]

-
S. Z. S. Al Ghafri, C. Revell, M. D. Lorenzo, G. Xiao, C. E. Buckley, E. F. May, and M. Johns, "Techno-economic and environmental assessment of LNG export for hydrogen production", International Journal of Hydrogen Energy, Vol. 48, No. 23, 2023, pp. 8343-8369.
[https://doi.org/10.1016/j.ijhydene.2022.11.160]

-
Y. Xin, Y. Zhang, P. Xue, K. Wang, E. Adu, and P. Tontiwachwuthikul, "The optimization and thermodynamic and economic estimation analysis for CO2 compression-liquefaction process of CCUS system using LNG cold energy", Energy, Vol. 236, 2021, pp. 121376.
[https://doi.org/10.1016/j.energy.2021.121376]

- J. M. Smith, H. C. Van Ness, M. M. Abbott, and M. T. Swihart, “Introduction to chemical engineering thermodynamics”, 8th ed., McGraw Hill, USA, 2018, pp. 327-343.
-
D. Y. Peng and D. B. Robinson, "A new two-constant equation of state", Industrial & Engineering Chemistry Fundamentals, Vol. 15, No. 1, 1976, pp. 59-64.
[https://doi.org/10.1021/i160057a011]

-
C. H. Twu, D. Bluck, J. R. Cunningham, and J. E. Coon, “A cubic equation of state with a new alpha function and a new mixing rule”, Fluid Phase Equilibria, Vol. 69, 1991, pp. 33-50.
[https://doi.org/10.1016/0378-3812(91)90024-2]