수지상 폴리(알릴렌 이써 설폰)에 도입된 지방족 알킬사슬 연결자길이에 따른 음이온교환막의 특성 연구
2022 The Korean Hydrogen and New Energy Society. All rights reserved.
Abstract
Recently, research on the development of anion exchange membranes (AEMs) has received considerable attention from the scientific community around the world. Here, we fabricated a series of AEMs with branched structures with different alkyl spacers and conducted comparative evaluations. The introduction of these branched structures is an attempt to overcome the low ionic conductivity and stability problems that AEMs are currently facing. To this end, branched polymers with different spacer lengths were synthesized and properties of each membrane prepared according to the branched structure were compared. The chemical structure of the polymer was investigated by proton nuclear magnetic resonance, Fourier transform infrared, and gel permeation chromatography, and the thermal properties were investigated using thermogravimetric analysis. The branched anion exchange membrane with (CH2)3 and (CH2)6 spacers exhibited ionic conductivities of 8.9 mS cm-1 and 22 mS cm-1 at 90℃, respectively. This means that the length of the spacer affects the ionic conductivity. Therefore, this study showing the effect of the spacer length on the ionic conductivity of the membrane in the polymer structure constituting the ion exchange membrane is judged to be very useful for future application studies of AEM fuel cells.
Keywords:
Fuel cell, Anion exchange membrane, Branched structure, Spacer, Ion conductivity키워드:
연료전지, 음이온교환막, 수지상 구조, 연결자, 이온 전도도1. 서 론
산업혁명 이후에 급격히 증가된 화석연료 사용으로 인한 기후변화 및 환경오염이 전 지구의 문제로 대두되어 왔으며, 더불어 최근 인간들의 많은 활동으로 야기되는 온실가스의 배출을 줄이기 위해 온실가스의 순 배출량이 0 (zero)으로 수렴하도록 하는 ‘탄소중립(net zero)’이 국제사회의 기후위기 대응 목표가 되었다. 이러한 분위기에 발맞춰 우리나라는 최근 탄소중립을 목표로 ‘기후위기 대응을 위한 탄소중립·녹색성장 기본법’을 제정하기까지 이르렀으며, 다양한 분야에서 친환경적인 국제사회를 이룩하기 위해 노력 중에 있다.
환경 친화적인 사회구현이라는 시대적 흐름 아래, 연료전지는 화학에너지를 전기에너지로 변환시키는 발전장치1,2)이며, 이는 연소 엔진에 비해 온실가스 배출이 적은 매우 효율적인 장치로서 많은 과학자들의 관심을 받고 있다. 연료전지는 연료극(anode)에 주입된 수소가 산화반응을 통해 수소이온과 전자로 분리되고 공기극(cathode)으로 주입된 공기와 만나 물을 생성하게 된다. 이때, 분리된 전자의 이동으로 연료전지는 전기를 발생시키게 된다3-5).
이러한 연료전지는 작동온도에 따라 고온형과 저온형으로 나눌 수 있으며, 고온형 연료전지는 고출력 및 높은 발전효율을 가지지만 시동시간이 오래 걸리며, 저온형 연료전지는 부하 변동성이 뛰어나고 시동시간이 짧지만 고가의 백금전극을 필요로 한다6,7).
저온형 연료전지 중 음이온교환막연료전지(anion exchange membrane fuel cell, AEMFC)는 양이온교환막연료전지(proton exchange membrane fuel cell, PEMFC), 알칼라인연료전지(alkaline fuel cell, AFC)와 비교하였을 때, 여러 가지 장점을 갖고 있다8-11). 먼저, 빠른 산소환원 반응으로 높은 에너지효율을 가지며, 비백금 및 비귀금속 촉매 사용이 가능하여 PEMFC와 비교했을 때, 비용적인 면에서 연료전지의 가격을 낮추는 요인을 갖고 있다. 또한, 액체 전해질을 사용하는 AFC 운전 시 탄산 포타슘(K2CO3)의 침전으로 인한 문제, 즉 연료극에서 반응하는 수산화이온(hydroxyl ion, OH)의 수를 저해시키면서 가스확산층(gas diffusion layer)의 미세구멍(pore)을 막는 등과 같은 연료전지의 성능을 감소시키는 단점을 보완할 수 있다12-14).
이러한 장점으로 많은 유형의 AEM이 현재 연료전지 응용을 위해 개발되고 있으며, 연구개발은 주사슬의 구조를 변화시키거나 신규 작용기를 합성하여 작용기에 변화를 주는 연구들이 주를 이루고 있다. 특히, 주사슬을 빗 모양 구조로 변화시키거나 교차 연결(cross-linked)시키는 구조 및 수지상 구조를 사용하거나 무기 나노필러를 전해질 막에 혼합하여 도입시키는 것과 같은 전략들이 연료전지에 실제로 적용하기 위해 그리고 장시간 사용을 위해 연구되고 있다. 그러나 많은 연구와 노력에도 불구하고 아직까지 AEMFC의 상용화의 어려움은 여전히 남아있는 상태이다15-19).
상용화를 막는 주요인은 음이온교환막 연료전지의 낮은 성능과 낮은 안정성으로 볼 수 있다. 이 중 연료전지의 성능과 직결된 요인은 낮은 이온전도도이다. 낮은 이온전도도의 성능을 향상시키기 위해 많은 양이온 작용기를 도입하게 되면, 전도성은 높아지더라도 오히려 물 흡수가 높아지고 결국 막의 치수안정성 및 성능저하를 유발하게 된다. 이러한 문제점을 극복하기 위해서 친수성/소수성 미세 상 분리를 향상시켜 이온전도성을 높이면서 알칼리 조건에서 내성이 있는 막을 제조하기 위한 주 사슬 구조에 수지상 구조를 도입하는 연구들이 활발히 진행 중이다. 수지상 구조의 고분자 매트릭스는 몇 가지 특성을 나타낸다. 수지상 구조는 알칼리 환경에서 OH⁻공격에 대해 입체장해 효과를 가지면서 고분자 사슬 간의 간격을 유지하고 움직임을 억제하여 막의 팽창을 막는 동시에 물 분자를 저장할 수 있는 자유체적을 확보할 수 있다. 앞서 언급되었던 연료전지의 성능과 직결되는 요소인 이온전도성을 높이기 위해 이러한 자유체적을 확보하는 것은 매우 중요하며, 수지상 구조는 자유체적을 확보하는 데 매우 효과적인 방법이다20-23).
다른 요인은 알칼리 조건에서 나타나는 낮은 안정성이다. 이는 호프만제거반응(E2)과 친핵성치환반응(SN2)에 의해 주로 나타나는 것으로 이를 해결하기 위해서는 알킬암모늄염(alkyl ammonium salt)을 보다 큰(bulky) 양이온으로 대체하여 SN2 반응성을 줄이는 것이다. 또는 길고 유연한 알킬사슬 연결자를 이용하여 고분자 주 사슬로부터 양이온 작용기를 분리하는 것은 양이온 작용기의 이동성을 증가시키고 이는 확실하게 막의 뚜렷한 이온클러스터의 형성을 유리하게 만들며, 막 내 물 분자의 이동을 향상시키게 된다. 따라서 전해질 막의 분해에 대해 덜 유리한 환경을 만들어낼 수 있다24,25).
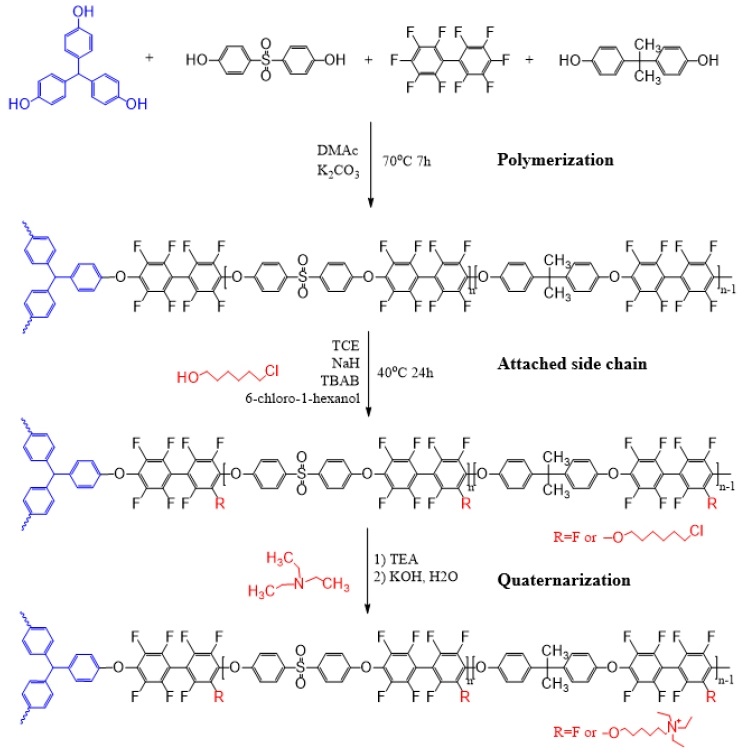
본 연구는 앞서 소개한 두 가지 전략을 접목하여 연료전지의 성능과 밀접한 관련이 있는 수지상 구조의 고분자 매트릭스에 고분자 주사슬과 알킬암모늄염 사이에 위치한 메틸렌사슬의 길이((CH2)n에서 n=3과 6)를 달리하여 제조한 후, 이들의 성능을 비교하고자 하였다(Fig. 1). 고분자 매트릭스의 수지상 정도(degree of branching)는 과도한 얽힘으로 인한 막의 물성 및 성능저하를 방지하기 위해 3%로 설정하여 실험하였으며, 합성된 고분자의 화학적 구조, 열적 특성 분석, 이온전도도 등을 통하여 음이온교환막으로서의 유용성을 입증하고자 하였다.
2. 실 험
2.1 시약
Bis(4-hydroxyphenyl)sulfone (BHS, 99%), decafluorobiphenyl (DFB, 98%), 4,4′,4″-trihydroxytriphenylmethane (THTPM), 6-chloro-1-hexanol (98%), tetrabutylammonium bromide (TBAB, 98%)는 TCI 사(Tokyo, Japan)에서, bispheol A (BPA, 97%), triethylamine (TEA, 99%)은 Alfa Aeasar 사(Haverhill, MA, USA)에서 구입하여 사용하였다. 그리고 sodium hydride (NaH, 60% dispersion in mineral oil), N,N-dimethylacetamide (DMAc, anhydrous, 99.8%), chloroform-d (CDCl3, 99.8 atom% D, contains 0.03% [v/v] TMS)는 Sigma-Aldrich 사(St. Louis, MO, USA)에서 구매하여 사용하였다. Potassium carbonate (anhydrous K2CO3, 99.5%), potassium hydroxide (KOH, 95%), 에탄올, 메탄올, 아세톤 및 따로 언급하지 않은 용매는 Samchun Chemicals (Seoul, Korea)에서 구매하여 사용하였고, 1,1,2,2-tetrachloroethane (TCE, 98%)은 대정화금(Siheung, Korea)에서 구매하여 사용하였다.
2.2 수지상 poly(arylene ether sulfone) (BPAES) 랜덤 공중합체의 합성
수지상 poly(arylene ether sulfone) 랜덤 공중합체의 합성은 다음과 같다. 100 mL의 둥근바닥 플라스크에 DFB (2.24 g, 6.7 mmol), BHS (1 g, 2.0 mmol), BPA (1.06 g, 4.7 mmol), THTPM (0.058 g, 0.2 mmol), 그리고 K2CO3 (3.74 g, 27 mmol)를 넣고 DMAc (12 mL)와 함께 질소 분위기 하에서 7시간 동안 교반하였다. 합성된 고분자를 메탄올/아세톤/3차 증류수(DI water) (6:1:1, v/v/v)의 혼합 용매에 부어, 하얀 실선 형태 고체를 얻었다. 이후, 회수한 고분자를 60℃ 건조 오븐에 넣고, 24시간 동안 고분자 내에 남아있는 용매를 완전히 건조하였다. 제조한 BPAES의 수평균분자량(Mn), 중량평균분자량(Mw) 및 다분산지수(polydisperse index, PDI)은 각각 12,400, 117,300 및 9.4였다.
한편, 비교시료로 사용된 선형의 고분자(PAES-3와 PAES-6)는 위 제조 방법에서 THTPM을 포함시키지 않은 반응물로부터 위와 동일한 방법을 사용하여 제조하였다.
2.3 연결자가 도입된 수지상 poly(arylene ether sulfone) (BPAES-x)의 합성
BPAES에 (CH2)6가 연결된 BPAES-6의 합성방법은 다음과 같다. 100 mL 둥근바닥 플라스크에 건조한 BPAES (1 g, 0.9 mmol)와 TCE (18 mL)를 넣고, 질소 가스 아래 40℃에서 2시간 동안 교반시키고, TCE (3 mL)에 TBAB (0.20 g, 6.4 mmol)와 NaH (0.62 g, 25.7 mmol)를 녹여 플라스크에 첨가하였다. 이후, 6-chloro-1-hexanol (3.4 mL)을 천천히 첨가하고, 이 반응을 40℃에서 24시간 동안 지속하였다. 반응이 끝난 후, 메탄올 및 3차 증류수를 이용하여 씻어낸 다음, 재결정하여 하얀 분말 고체를 얻었다. 생성물은 60℃의 건조 오븐에서 24시간 동안 건조하였다26-29).
한편, (CH2)3가 연결된 BPAES-3의 합성방법은 6-chloro-1-hexanol 대신에 3-chloro-1-propanol을 사용하여, 위에서와 실시한 동일한 반응절차를 거쳐서 BPAES-3을 제조하였다.
2.4 제막 및 4차 암모늄화 반응
연결자가 도입된 BPAES 막은 4차 암모늄화 반응을 위해 다음과 같이 준비하였다. 완전히 건조된 사슬이 도입된 BPAES (0.2 g)를 TCE (10 mL)에 40℃에서 8시간 동안 교반하여 완전히 용해시켰다. 이후, 평평한 유리판에 직접 캐스팅하여 70℃의 오븐에서 용매가 날아갈 때까지 완전히 건조하였다. 이후, 제조된 막은 3차 증류수를 이용하여 유리판으로부터 떼어내고 TEA 35 wt%에 24시간 동안 40℃에서 담지하는 방식으로 4차 암모늄염화 반응을 진행하였다. 제조한 막들의 두께는 26-30 µm였다.
2.5 특성 분석
분자량(Mn과 Mw) 및 PDI(Mw/Mn)의 확인은 HLC-8320 (Tosoh Corporation, Tokyo, Japan)에 의해 측정하였고, 합성된 고분자의 구조분석을 위해 1H NMR (CDCl3)및 FT-IR (KBr/film) 분석을 진행하였으며, 각각 핵자기공명분광법(JNM-ECA600, JEOL Ltd, Tokyo, Japan) 및 푸리에 변환 적회선(Fourier MIR/NIR spectrometer, Perkin Elmer, Waltham, MA, USA) 스펙트럼 기기를 사용하여 수행하였다.
열중량분석(thermogravimetric analysis, TGA)은 TA Instruments (Q50)에 의해 분당 10℃씩 온도를 높여 800℃까지 측정하였으며, 전기화학적 특성평가는 교류 임피던스 분광기(conductivity Test Bench, SciTech Korea, Seoul, Korea)를 이용하여 측정하였다. 이온전도도는 다음의 식(1)로 계산하였다.
| (1) |
여기서 σ은 이온전도도(mS cm-1), L은 전극 사이의 길이, W와 T는 각각 너비(cm)와 두께(cm)를 말하며, R은 두 전극 사이의 저항값(Ω)을 나타낸다.
3. 결과 및 고찰
3.1 고분자의 합성과 구조분석
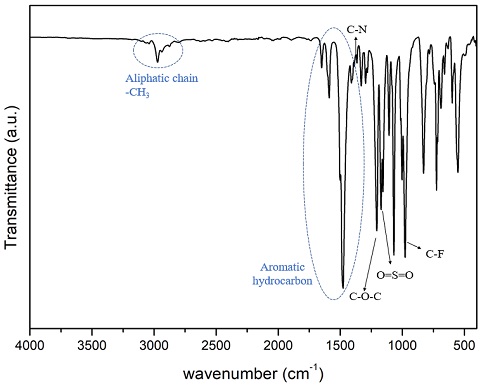
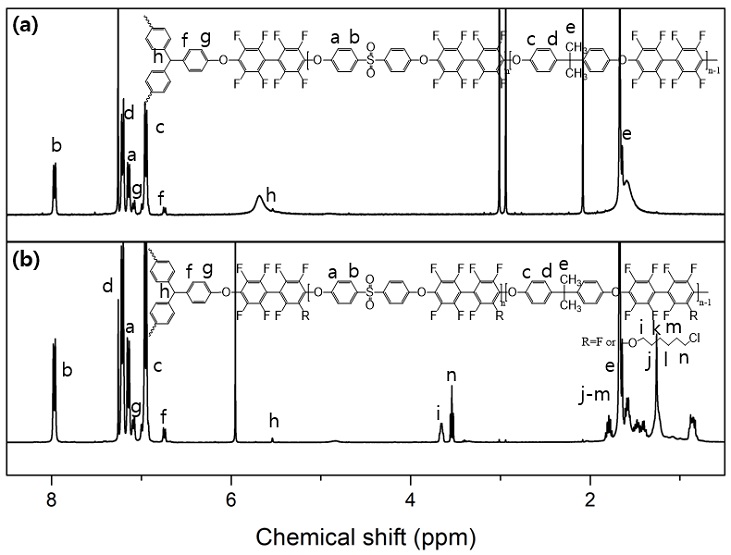
BPAES 및 연결자가 도입된 BPAES의 합성은 친핵성치환반응에 의해 성공적으로 합성되었으며 그 과정을 Fig. 1에 나타내었다. 또한, FT-IR 측정을 통해 고분자의 합성 여부를 확인하였으며(Fig. 2), 연결자 도입 후 고분자의 면밀한 구조분석을 위해 1H NMR을 측정하여 연결자의 도입을 확인하고 그 결과를 Fig. 3에 나타내었다.
먼저, Fig. 2에 나타난 FT-IR 스펙트럼에서 2,900-3,050 cm-1의 범위는 연결자 및 BPA의 methyl기에 해당하는 피크임을 확인하였으며 1,649 cm-1, 1,589 cm-1 및 1,477 cm-1의 피크는 방향족 탄화수소(벤젠 고리)에 상응하는 신축진동임을 확인하였다. 또한, 1,205 cm-1, 1,156 cm-1, 1,171 cm-1 및 977 cm-1은 각각 이써 결합의 비대칭 신축진동, sulfone의 신축진동, C-F의 신축진동임을 나타내는 것을 확인하였으며, C-N 신축진동에 해당하는 피크가 1,365 cm-1에서 관찰됨을 확인하였다.
Fig. 3의 1H NMR 스펙트라를 보면, 합성한 BPAES 랜덤 공중합체의 주 사슬에 위치한 양성자 피크는 6.5-8.5 ppm 사이에서 나타났고, BPA의 methyl 그룹 양성자 피크는 1.6 ppm에서, THTPM의 methine 양성자 피크는 약 5.5 ppm에서 나타남을 확인하였다. 또한 주 사슬에 연결자 도입 이후 지방족 알킬기의 양성자 피크는 0.9-1.9 ppm 사이에서 확인되었으며, 특히 주 사슬과 Cl 원자 사이에 존재하는 methylene 양성자 피크는 3.4-3.9 ppm 사이에서 확인하였다. 대표적인 화학구조에 대한 각 양성자에 해당하는 구체적인 피크해석은 Fig. 3에 나타내었다25,30-33).
3.2 고분자의 용해도 시험
본 연구에서 합성된 고분자 BPAES 및 BPAES-6의 다양한 용매에 대한 용해도를 측정하였다. 용해도 측정은 10 wt% 농도로 진행하였다. 본 실험에서 제조된 고분자는 증류수, 메탄올과 같은 극성 양성자성 용매에는 용해되지 않았고, 클로로포름, DMF와 같은 극성 비 양성자성 용매에는 완전히 용해되었으나, DMSO에서는 용해되지 않는 특성을 보였다(Table 1)34).
3.3 열적 특성
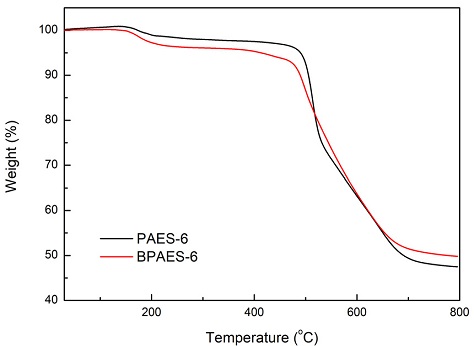
합성한 고분자의 열적 특성은 실온에서 분당 10℃씩 800℃까지 온도를 상승시켜 TGA를 측정하여 평가하였다(Fig. 4)35,36). 비교군으로 사용된 (CH2)6 연결자를 가진 선형 고분자(PAES-6)의 TGA 그래프를 보면, 150℃ 범위에서 첫 번째 무게손실이 일어나고, 500℃ 범위에서 두 번째 무게손실이 일어난 것을 보여준다. 또한, (CH2)6 연결자를 가진 수지상 고분자(BPAES-6)의 TGA 그래프 또한 150℃ 범위 및 470℃ 범위에서 무게손실이 일어나며 이들은 각각 작용기 및 주 사슬의 분해에서 나타나는 두 번에 걸친 무게손실임을 확인할 수 있다.
두 TGA 그래프를 비교하면, 수지상 고분자(BPAES-6)에 비해 비교 고분자(PAES-6)의 열적분해가 가파른 경사를 보이며 빠르게 진행됨을 볼 수 있는데, 이는 가지가 있는 수지상 고분자의 입체장해 및 자유체적 확보로 인한 보다 큰 부피를 갖는 특성에 기인한 것으로 수지상 고분자가 열적으로 더 안정함을 예측할 수 있으며 또한 위의 결과로부터 수지상 고분자의 주 사슬에 작용기가 성공적으로 도입되었음을 확인할 수 있었다.
3.4 이온전도도 및 활성화 에너지
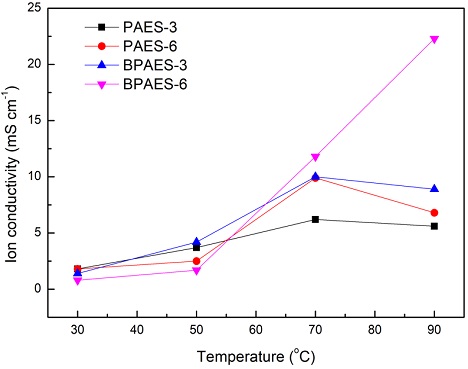
음이온교환막의 이온전도도는 연료전지의 실질적 적용에 있어 매우 중요한 요소로서 작용기의 종류 및 고분자의 형태 등 매우 다양한 요인에 의해 결정된다37-39). 본 연구에서는 수지상 구조를 포함한 BPAES-3 및 BPAES-6 이외에 수지상 구조를 포함하지 않은 선형의 고분자 형태인 PAES-3과 PAES-6을 준비하여 비교하고자 하였다. 준비된 모든 막들의 두께는 30 µm 이하였으며 이온전도도는 100% 가습 조건의 다양한 온도 범위에서 측정 및 분석하여 그 결과를 Fig. 5에 나타내었다.
이온전도도는 온도가 높아짐에 따라 그 값이 증가하는 양상을 보이게 되는데, 이는 온도 증가로 인해 이온이 쉽게 확산되고, 막이 보유하는 자유체적이 높을수록 이온 확산이 증가하여 이온수송에 더 유리한 환경을 만들기 때문이라고 예측된다. 그러나 90℃에서 BPAES-6을 제외한 측정된 모든 막에서 이온전도도 감소를 나타내었다. 이는 높은 온도에서 막이 녹거나 붕괴되는 현상에 기인한 것으로, 고온에서 작동 시 충분한 내구성을 갖지 못한 것임을 예측할 수 있다. 또한, 수지상 구조를 포함하지 않는 PAES 막의 이온전도도는 BPAES 막의 이온전도도보다 전체적으로 낮음을 확인할 수 있는데, 이는 수지상 구조가 가지는 물을 보유할 수 있는 자유체적이 선형의 구조보다 많아서 다량의 이온을 이동시킬 수 있는 이온전도 채널을 보유한다는 것을 의미한다. 특히, 같은 수지상 구조의 막에서 연결자의 길이가 (CH2)3인 막(BPAES-3)의 이온전도도는 90℃에서 8.9 mS cm-1, (CH2)6인 막(BPAES-6)의 이온전도도는 90℃에서 22 mS cm-1로 연결자의 길이가 긴 BPAES-6의 이온전도도가 높은데, 이는 수지상 구조가 보유한 자유체적 내에서도 긴 사슬이 자가조립에 의해 이온전도에 유리한 환경을 제공하기 때문이라고 예상된다40,41).
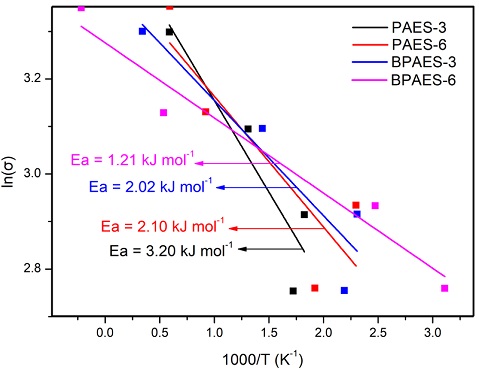
준비된 막들의 활성화 에너지(Ea)는 Arrhenius plot의 기울기로부터 계산되었으며, Fig. 6에 나타내었다. 활성화 에너지는 막 내를 통과하는 이온의 이동 메커니즘을 예측할 수 있으며, 본 연구에서 준비된 막들의 활성화 에너지가 15 kJ mol-1 이하를 나타내기 때문에, vehicle 메커니즘을 통해 이온의 이동이 우세하게 이루어짐을 예측할 수 있다42,43).
4. 결 론
본 연구에서는 연료전지 성능을 높일 수 있는 두 가지 전략을 접목하여 새로운 음이온교환 막을 개발하고자 하였다. 수지상 구조의 고분자 매트릭스에 (CH2)3 및 (CH2)6 길이의 연결자를 도입하였으며 수지상 구조의 도입으로 막 내의 수분을 보유할 수 있는 자유체적을 높임과 동시에 (CH2)6 길이의 연결자는 막 내 자가조립을 통해 넓은 이온수송 채널을 형성하여 이온전도에 유리한 환경을 제공할 것이다. 그 결과 적절한 길이의 연결자를 가진 BPAES-6의 수산화이온전도도는 제조된 다른 막에 비해 90℃에서 22 mS cm-1의 높은 값을 나타내는 것을 확인하였다. 이러한 결과는 연결자의 길이가 이온전도도에 영향을 미친다는 것을 의미하며, 이러한 수지상을 이용한 연구는 AEMFC의 응용연구에 매우 유용하다고 판단된다.
Acknowledgments
이 성과는 2020년도 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구입니다(No. 2020R1A2B5B01001458).
References
-
H. Wang, J. Zhang, X. Ning, M. Tian, Y. Long, and S. Ramakrishna, “Recent advances in designing and tailoring nanofiber composite electrolyte membranes for high-performance proton exchange membrane fuel cells”, Int. J. Hydrogen Energy, Vol. 46, No. 49, 2021, pp. 25225-25251.
[https://doi.org/10.1016/j.ijhydene.2021.05.048]

-
H. Y. Son, J. S. Han, and S. S. Yu, “Development of a multi-physics model of polymer electrolyte membrane muel cell using aspen custom modeler”, Trans Korean Hydrogen New Energy Soc, Vol. 32, No. 6, 2021, pp. 489-496.
[https://doi.org/10.7316/KHNES.2021.32.6.489]

-
A. R. Kim, M. Vinothkannan, S. Ramakrishnan, B. H. Park, M. K. Han, and D. J. Yoo, “Enhanced electrochemical performance and long-term durability of composite membranes through a binary interface with sulfonated unzipped graphite nanofibers for polymer electrolyte fuel cells operating under low relative humidity”, Appl. Surf. Sci., Vol. 593, 2022, pp. 153407.
[https://doi.org/10.1016/j.apsusc.2022.153407]

-
J. Y. Chu, K. H. Lee, A. R. Kim, and D. J. Yoo, “Graphene-mediated organic-inorganic composites with improved hydroxide conductivity and outstanding alkaline stability for anion exchange membranes”, Composities Part B, Vol. 164, 2019, pp. 324-332.
[https://doi.org/10.1016/j.compositesb.2018.11.084]

-
G. Gupta, S. Sharma, and P. M. Mendes “Nafion-stabilised bimetallic Pt–Cr nanoparticles as electrocatalysts for proton exchange membrane fuel cells (PEMFCs)”, RCS Advances, Vol. 6, No. 86, 2016, pp. 82635-82643.
[https://doi.org/10.1039/C6RA16025E]

-
B. H. Oh, A. R. Kim, and D. J. Yoo, “Profile of extended chemical stability and mechanical integrity and high hydroxide ion conductivity of poly(ether imide) based membranes for anion exchange membrane fuel cells”, Int. J. Hydrogen Energy, Vol. 44, No. 8, 2019, pp. 4281-4292.
[https://doi.org/10.1016/j.ijhydene.2018.12.177]

-
S. K. Ryu, M. Vinothkannan, A. R. Kim, and D. J. Yoo, “Effect of type and stoichiometry of fuels on performance of polybenzimidazole-based proton exchange membrane fuel cells operating at the temperature range of 120–160 °C’’, Energy, Vol. 238, 2022, pp. 121791.
[https://doi.org/10.1016/j.energy.2021.121791]

-
W. E. Mustain, M. Chatenet, M. Page, and Y. S. Kim, “Durability challenges of anion exchange membrane fuel cells”, Energy & Environmental Science, Vol. 13, No. 9, 2020, pp. 2805-2838.
[https://doi.org/10.1039/D0EE01133A]

-
D. R. Dekel, “Review of cell performance in anion exchange membrane fuel cells”, J. Power Sources, Vol. 375, 2018, pp. 158-169.
[https://doi.org/10.1016/j.jpowsour.2017.07.117]

-
P. G. Santori, F. D. Speck, S. Cherevko, H. A. Firousjaie, X. Peng, W. E. Mustain, and F. Jaouen, “High performance FeNC and Mn-oxide/FeNC layers for AEMFC cathodes”, J. Electrochem. Soc., Vol. 167, No. 13, 2020, pp. 134505.
[https://doi.org/10.1149/1945-7111/abb7e0]

-
H. A. Firouzjaie and W. E. Mustain, “Catalytic advantages, challenges, and priorities in alkaline membrane fuel cells”, ACS Catal., Vol. 10, No. 1, 2020, pp. 225-234.
[https://doi.org/10.1021/acscatal.9b03892]

-
G. Merle, M. Wessling, and K. Nijmeijer, “Anion exchange membranes for alkaline fuel cells: a review“, Journal of Membrane Science, Vol. 377, No. 1-2, 2011, pp. 1-35.
[https://doi.org/10.1016/j.memsci.2011.04.043]

-
F. Xu, Y. Su, and B. Lin, “Progress of alkaline anion exchange membranes for fuel cells: the effects of micro-phase separation”, Frontiers in Materials, Vol. 7, No. 4, 2020, pp. 1-7.
[https://doi.org/10.3389/fmats.2020.00004]

-
Y. Luo, Y. Wu, B. Li, T. Mo, Y. Li, S. P. Feng, J. Qu, and P. K. Chu, “Development and application of fuel cells in the automobile industry”, Journal of Energy Storage, Vol. 42, 2021, pp. 103124.
[https://doi.org/10.1016/j.est.2021.103124]

-
J. Sang, L. Yang, Z. Li, F. Wang, Z. Wang, and H. Zhu, “Comb-shaped SEBS-based anion exchange membranes with obvious microphase separation morphology”, Eelctrochimica Acta, Vol. 403, 2022, pp. 139500.
[https://doi.org/10.1016/j.electacta.2021.139500]

-
F. Liu, S. Wang, J. Li, X. Wang, Z. Yong, Y. Cui, D. Liang, and Z. Wang, “Novel double cross-linked membrane based on poly (ionic liquid) and polybenzimidazole for high-temperature proton exchange membrane fuel cells”, Journal of Power Sources, Vol. 515, 2021, pp. 230637.
[https://doi.org/10.1016/j.jpowsour.2021.230637]

-
Q. Ge, X. Liang, L. Ding, J. Hou, J. Miao, B. Wu, Z. Yang, and T. Xu, “Guiding the self-assembly of hyperbranched anion exchange membranes utilized in alkaline fuel cells”, Journal of Membrane Science, Vol. 573, 2019, pp. 595-601.
[https://doi.org/10.1016/j.memsci.2018.12.049]

-
K. H. Lee, J. Y. Chu, A. R. Kim, and D. J. Yoo, “Effect of functionalized SiO2 toward proton conductivity of composite membranes for PEMFC application”, Int. J. Energy Res., Vol. 43, No. 10, 2019, pp. 5333-5345.
[https://doi.org/10.1002/er.4610]

-
J. Y. Chu, K. H. Lee, A. R. Kim, and D. J. Yoo, “Improved electrochemical performance of composite anion exchange membranes for fuel cells through cross linking of the polymer chain with functionalized graphene oxide”, Journal of Membrane Science, Vol. 611, 2020, pp. 118385.
[https://doi.org/10.1016/j.memsci.2020.118385]

-
J. Liu, X. Yan, L. Gao, L. Hu, X. Wu, Y. Dai, X. Ruan, and G. He, “Long-branched and densely functionalized anion exchange membranes for fuel cells”, Journal of Membrane Science, Vol. 581, 2019, pp. 82-92.
[https://doi.org/10.1016/j.memsci.2019.03.046]

-
K. Wang, Q. Wu, X. Yan, J. Liu, L. Gao, L. Hu, N. Zhang, Y. Pan, W. Zheng, and G. He, “Branched poly(ether ether ketone) based anion exchange membrane for H2/O2 fuel cell”, Int. J. Hydrogen Energy, Vol. 44, No. 42, 2019, pp. 23750-23761.
[https://doi.org/10.1016/j.ijhydene.2019.07.080]

-
X. L. Gao, Q. Yang, H. Y. Wu, Q. H. Sun, Z. Y. Zhu, Q. G. Zhang, A. M. Zhu, and Q. L. Liu, “Orderly branched anion exchange membranes bearing long flexible multi-cation side chain for alkaline fuel cells”, Journal of Membrane Science, Vol. 589, 2019, pp. 117247.
[https://doi.org/10.1016/j.memsci.2019.117247]

-
A. Sannigrahi, S. Takamura, and P. Jannasch, “Block copolymers combining semi-fluorinated poly(arylene ether) and sulfonated poly(arylene ether sulfone) segments for proton exchange membranes”, Int. J. Hydrogen Energy, Vol. 39, No. 28, 2014, pp. 15718-15727.
[https://doi.org/10.1016/j.ijhydene.2014.07.155]

-
A. H. N. Rao, S. Y. Nam, and T. H. Kim, “Comb-shaped alkyl imidazolium-functionalized poly(arylene ether sulfone)s as high performance anion-exchange membranes”, Journal of Materials Chemistry A, Vol. 3, No. 16, 2015, pp. 8571-8580.
[https://doi.org/10.1039/C5TA01123J]

-
H. S. Dang and P. Jannasch, “Exploring different cationic alkyl side chain designs for enhanced alkaline stability and hydroxide ion conductivity of anion-exchange membranes”, Macromolecules, Vol. 48, No. 16, 2015, pp. 5742-5751.
[https://doi.org/10.1021/acs.macromol.5b01302]

-
C. X. Lin, X. L. Huang, D. Guo, Q. G. Zhang, A. M. Zhu, M. L. Ye, and Q. L. Liu, “Side-chain-type anion exchange membranes bearing pendant quaternary ammonium groups via flexible spacers for fuel cells”, J. Mater. Chem. A, Vol. 4, No. 36, 2016, pp. 13938-13948.
[https://doi.org/10.1039/C6TA05090E]

-
A. D. Mohanty, S. E. Tignor, J. A. Krause, Y. K. Choe, and C. Bae, “Systematic alkaline stability study of polymer backbones for anion exchange membrane applications”, Macromolecules, Vol. 49, No. 9, 2016, pp. 3361-3372.
[https://doi.org/10.1021/acs.macromol.5b02550]

-
E. N. Hu, C. X. Lin, F. H. Liu, X. Q. Wang, Q. G. Zhang, A. M. Zhu, and Q. L. Liu, “Poly(arylene ether nitrile) anion exchange membranes with dense flexible ionic side chain for fuel cells”, Journal of Membrane Science, Vol. 550, 2018, pp. 254-265.
[https://doi.org/10.1016/j.memsci.2018.01.010]

-
M. Niu, C. Zhang, G. He, F. Zhang, and X. Wu, “Pendent piperidinium-functionalized blend anion exchange membrane for fuel cell application”, Int. J. Hydrogen Energy, Vol. 44, No. 29, 2019, pp. 15482-15493.
[https://doi.org/10.1016/j.ijhydene.2019.04.172]

-
X. Gong, X. Yan, T. Li, X. Wu, W. Chen, S. Huang, Y. Wu, D. Zhen, and G. He, “Design of pendent imidazolium side chain with flexible ether-containing spacer for alkaline anion exchange membrane”, Journal of Membrane Science, Vol. 523, 2017, pp. 216-224.
[https://doi.org/10.1016/j.memsci.2016.09.050]

-
X. Q. Wang, C. X. Lin, F. H. Liu, L. Li, Q. Yang, Q. G. Zhang, A. M. Zhu, and Q. L. Liu, “Alkali-stable partially fluorinated poly(arylene ether) anion exchange membranes with a claw-type head for fuel cells”, J. Mater. Chem. A, Vol. 6, No. 26, 2018, pp. 12455-12465.
[https://doi.org/10.1039/C8TA03437K]

-
Y. Xu, N. Ye, D. Zhang, Y. Yang, J. Yang, and R. He, “Imidazolium functionalized poly(aryl ether ketone) anion exchange membranes having star main chains or side chains”, Renewable Energy, Vol. 127, 2018, pp. 910-919.
[https://doi.org/10.1016/j.renene.2018.04.077]

-
K. Wang, Z. Zhang, S. Li, H. Zhang, N. Yue, J. Pang, and Z. Jiang, “Side-chain-type anion exchange membranes based on poly(arylene ether sulfone)s containing high-density quaternary ammonium groups”, ACS Appl. Mater. Interfaces, Vol. 13, No. 20, 2021, pp. 23547-23557.
[https://doi.org/10.1021/acsami.1c00889]

-
D. J. Yoo, S. H. Hyun, A. R. Kim, G. G. Kumar, and K. S. Nahm, “Novel sulfonated poly(arylene biphenylsulfone ether) copolymers containing bisphenylsulfonyl biphenyl moiety: structural, thermal, electrochemical and morphological characteristics”, Polym. Int., Vol. 60, No. 1, 2011, pp. 85-92.
[https://doi.org/10.1002/pi.2914]

-
X. Li, K. Wang, D. Liu, L. Lin, and J. Pang, “Poly(arylene ether ketone) with tetra quaternary ammonium carbazole derivative pendant for anion exchange membrane”, Polymer, Vol. 195, 2020, pp. 122456.
[https://doi.org/10.1016/j.polymer.2020.122456]

-
J. Y. Chu, A. R. Kim, K. S. Nahm, H. K. Lee, and D. J. Yoo, “Synthesis and characterization of partially fluorinated sulfonated poly(arylene biphenylsulfone ketone) block copolymers containing 6F-BPA and perfluorobiphenylene units”, Int. J. Hydrogen Energy, Vol. 38, No. 14, 2013, pp. 6268-6274.
[https://doi.org/10.1016/j.ijhydene.2012.11.144]

-
A. N. Lai, P. C. Hu, J. W. Zheng, S. F. Zhou, L. Zhang, “Fluorene-containing poly(arylene ether sulfone nitrile)s multiblock copolymers as anion exchange membranes”, Int. J. Hydrogen Energy, Vol. 44, No. 44, 2019, pp. 24256-24266.
[https://doi.org/10.1016/j.ijhydene.2019.07.134]

-
J. S. Olsson, T. H. Pham, and P. Jannasch, “Tuning poly(arylene piperidinium) anion-exchange membranes by copolymerization, partial quaternization and crosslinking”, Journal of Membrane Science. Vol. 578, 2019, pp. 183-195.
[https://doi.org/10.1016/j.memsci.2019.01.036]

-
S. Gahlot and V. Kulshrestha, “Dramatic improvement in water retention and proton conductivity in electrically aligned functionalized CNT/SPEEK nanohybrid PEM”, ACS Appl. Mater. Interfaces, Vol. 7, No. 1, 2015, pp. 264-272.
[https://doi.org/10.1021/am506033c]

-
M. Fang, D. Liu, S. Neelakandan, M. Xu, D. Liu, and L. Wang, “Side-chain effects on the properties of highly branched imidazolium-functionalized copolymer anion exchange membranes”, Applied Surface Science, Vol. 493, 2019, pp. 1306-1316.
[https://doi.org/10.1016/j.apsusc.2019.07.059]

-
D. Liu, M. Xu, M. Fang, J. Chen, and L. Wang, “Branched comb-shaped poly(arylene ether sulfone)s containing flexible alkyl imidazolium side chains as anion exchange membranes”, J. Mater. Chem. A, Vol. 6, No. 23, 2018, pp. 10879.
[https://doi.org/10.1039/C8TA02115E]

-
K. D. Kreuer, A. Rabenau, and W. Weppner, “Vehicle mechanism, a new model for the interpretation of the conductivity of fast proton conductors”, Angewandte Chemie, Vol. 21, No. 3, 1982, pp. 208-209.
[https://doi.org/10.1002/anie.198202082]

-
K. H. Lee, J. Y. Chu, A. R. Kim, and D. J. Yoo, “Simultaneous improvement of anion conductivity and cell durability through the formation of dense ion clusters of F-doped graphitic carbon nitride/quaternized poly(phenylene oxide) composite membrane”, Journal of Membrane Science, Vol. 650, 2022, pp. 120384.
[https://doi.org/10.1016/j.memsci.2022.120384]