금속수소화물-팽창흑연 복합체의 열전달 특성 및 수소 저장 특성
2020 The Korean Hydrogen and New Energy Society. All rights reserved.
Abstract
Metal hydride is suitable for safe storage of hydrogen. The hydrogen storage kinetics of the metal hydride are highly dependent on its heat transfer characteristics. This study presents a metal hydride-expended graphite composite with improved thermal conductivity and its hydrogen storage kinetics. To improve the heat transfer characteristics, a metal hydride was mixed and compacted with a high thermal conductivity additive. As the hydrogen storage material, AB5 type metal hydride La0.9Ce0.1Ni5 was used. As an additive, flakes-type expended graphite was used. With improved heat transfer characteristics, the metal hydride-expended graphite composite stores hydrogen four times faster than metal hydride powder.
Keywords:
Metal hydride, Expended graphite, Thermal conductivity, Thermal diffusivity, Hydrogen storage키워드:
금속수소화물, 팽창흑연, 열전도도, 열확산도, 수소 저장1. 서 론
청정에너지로써 수소는 단위 중량당 에너지 밀도가 높고 전기와 같은 다른 에너지로의 변환이 용이하여 화석연료를 대체할 차세대 에너지원으로 각광받고 있다. 하지만 수소는 상온·상압에서 기체로 존재하기 때문에 수소를 다양한 분야에서 활용하기 위해서는 안전하며 경제적인 저장 기술이 필요하다.
수소 저장법은 상에 따라 기체 수소 저장, 액체 수소 저장, 고체 수소 저장으로 분류한다. 고체 수소 저장법 중 금속수소화물(metal hydride, MH)을 이용한 저장법은 수소 원자가 수소 분자의 반 데르 발스(Van der Walls) 반경보다 작은 간격으로 금속과 결합하여 MH를 형성하기 때문에 수소를 안전하게 저장하는 것이 가능하다1-3).
수소가 금속과 반응하여 MH를 형성하는 반응은 발열 반응이다. 수소 저장 시 발생한 열의 제거는 금속과 수소의 반응 속도를 높인다. MH에서 발생한 열을 효과적으로 제거하기 위해 MH가 장입된 수소 저장 용기에 핀(fin)4-6)이나 냉각 튜브7,8)를 적용하는 방법과 MH에 열전도도가 높은 첨가제를 혼합하는 방법이 사용되고 있다. 첨가제의 혼합은 MH의 열전달을 균일하게 향상시킬 뿐만 아니라 첨가제의 종류에 따라 수소의 이동경로를 제공하거나 성형체의 유지를 위한 바인더 기능을 부여할 수 있다. 열전도도가 높은 첨가제 중에서도 흑연은 밀도가 낮고 표면적이 넓어 MH와 혼합 시 이점이 있다. 또한 MH와 흑연을 혼합하고 압축하여 복합체를 제조하면 부피 저장 밀도가 향상되며 열전도도를 조절할 수 있다9-12). 수소 저장 용기에 장입된 복합체의 열전달은 MH의 팽창과 수축, 수소 가스의 유무 등 조건에 따라 변한다.
본 연구에서는 흑연 혼합 및 압축성형이 MH의 열전달 특성과 수소 저장 특성에 미치는 영향을 고찰하였다. MH와 흑연을 혼합하고 압축성형하여 복합체를 제조하였다. 복합체의 반지름 방향 열전도도 및 수소화 전후 유효 열전도도를 측정하였다. MH 분말과 선정된 복합체의 수소 저장 특성을 고찰하였다.
2. 실 험
2.1 LCN2-EG 복합체 선정
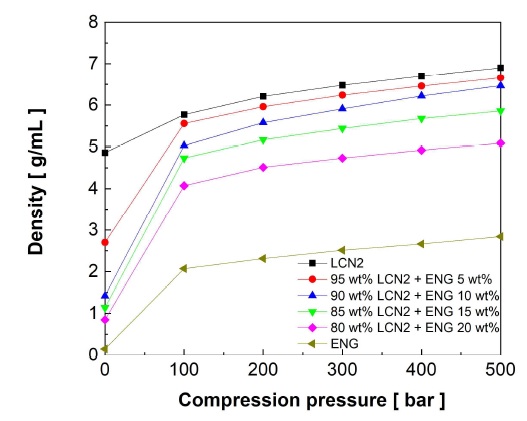
수소저장재로 수소 저장 특성이 우수한 AB5계 MH La0.9Ce0.1Ni5 (LCN2, Whole Win)을 선정하였다13). 첨가제로 열전도도가 우수한 플레이크 타입의 expended graphite (EG, Yanxin)를 선정하였다14). 분말 형태의 두 시료는 (100-x) wt% LCN2 – x wt% EG (x=0, 5, 10, 15, 20, 100)의 비율로 혼합되었으며, 복합체는 해당 혼합시료를 100, 200, 300 MPa로 압축하여 제조되었다. Fig. 1에 혼합시료와 복합체의 밀도를 나타내었다. 혼합시료 및 복합체의 밀도는 각각 탭 밀도(tap density) 및 겉보기 밀도로 측정되었다. EG의 혼합비가 증가할수록 혼합시료의 밀도가 급격히 감소하였다. 혼합시료를 압축성형한 복합체는 LCN2의 밀도에 근접하였다. EG의 혼합비가 증가할수록 복합체의 밀도가 감소하였다. 최소한의 에너지로 복합체 밀도를 LCN2의 95% 이상으로 유지하는 것을 고려하여 최적의 복합체로 100 MPa로 압축된 95 wt% LCN2 – 5 wt% EG가 선정되었다.
2.2 열전도도 측정 방법
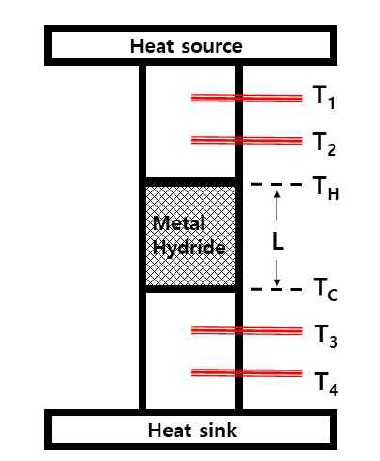
Fig. 2는 열전도도 측정 장치의 모식도이다. 열전도도 측정 장치에는 ASTM D5470의 간접 온도 측정법과 ASTM E1225의 단열 기법이 적용되었다. 가열부(heat source)와 냉각부(heat sink)에는 사각 기둥 구리 메타바(10 mm-L×10 mm-W)가 적용되었다. 각 메타바의 온도 측정부는 시료 접촉면에서 메타바의 축방향으로 10 mm와 20 mm 떨어진 곳에 위치한다. ASTM D5470의 간접 온도 측정법을 사용하기 위해서 동일한 물질을 높이가 다른 두 개의 사각 기둥으로 압축성형하여 시료(시료-1 : 10 mm-L×10 mm-W×10 mm-H, 시료-2 : 10 mm-L×10 mm-W×15 mm-H)를 준비하였다. 반지름 방향 열전도도를 측정을 위해 시료를 압축성형 방향과 직교하는 방향으로 위치시켜 높이와 열 임피던스(thermal impedance)를 측정하였다. 정상상태에 도달한 두 시료의 높이와 열 임피던스를 통해 측정시료의 열전도도를 산출하였다. 복합체의 열전도도 계산을 위해 사용된 식은 다음과 같다.
| (1) |
| (2) |
| (3) |
k : 열전도도(W/[m·K])
L : 시료의 높이(m)
θ : 열 임피던스([K·m2]/W)
A : 열전달 면적(m2)
QS : 시료 인가 열량(W)
QH : 가열부 열량(W)
QC : 냉각부 열량(W)
TH : 가열부 측 시료 표면 온도(℃)
TC : 냉각부 측 시료 표면 온도(℃)
2.3 열전달 특성 평가 방법 누락
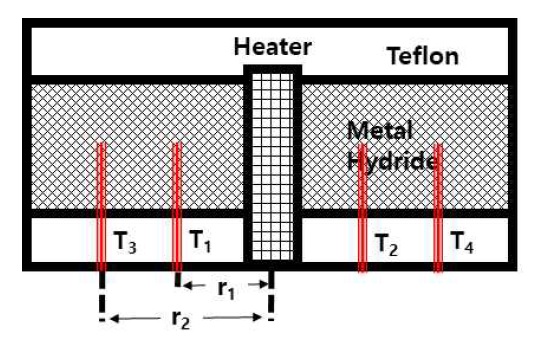
Fig. 3은 복합체의 열전달 및 수소 저장 특성 평가를 위해 구성한 장치의 모식도이다. 펄스(pulse) 형태로 열이 전달되는 현상을 분석하였으며 100 MPa로 압축된 95 wt% LCN2 – 5 wt% EG 복합체의 수소화 전후 열확산도를 측정하였다. 반응기 내부에 직경 54 mm 복합체가 장입될 수 있도록 제작 되었다. 복합체 중심에 약 6 mm 직경의 발열체를 설치하였다. 발열체를 이용하여 반복적으로 8.2 W의 열량을 5분간 공급하고 5분간 차단하였다. K 타입 열전대를 중심으로부터 반경 12.2 mm (1, 2번 지점)와 19.7 mm (3, 4번 지점)에 각각 설치하였다. 복합체의 상부와 하부에 테플론(teflon)을 두어 축방향 열전달을 줄였다. 반응기 외부에 20℃의 물을 순환시켜주었다. 시료는 3회 이상 수소 저장 및 방출을 진행하였다. 수소화 전은 진공상태이며 수소화 후는 40 bar의 수소가 공급된 상태이다. 수소화 전후 열확산도 계산식을 원통좌표계로 나타내면 다음과 같다.
| (4) |
| (5) |
T : 온도(K)
t : 시간(s)
α : 열확산도(mm2/s)
r : 반지름 길이(mm)
2.4 수소 저장 특성 평가 방법
수소 저장 특성 평가를 위해 2.3절에서 제시한 장치를 활용하였다. LCN2 분말(223.35 g)과 100 MPa로 압축된 95 wt% LCN2 – 5 wt% EG 복합체(223.37 g)를 사용하여 수소 저장 특성 평가를 진행하였다. 수소 저장 특성 평가 전 시료는 3회 이상의 수소 저장 및 방출을 통해 활성화되었다. 수소 저장 시 공급된 압력은 40 bar이며, 질량유량계를 이용하여 저장량을 평가하였다.
3. 결과 및 고찰
3.1 반지름 방향 열전도도
Fig. 4에 LCN2와 EG가 혼합된 분말과 LCN2-EG 복합체의 수직 방향 단면에 대한 scanning electron microscope ion mapping 결과를 나타내었다. Table 1에 MH 분말, LCN2 성형체(compact) 및 95 wt% LCN2 - 5 wt% EG 복합체의 반지름 방향 열전도도를 나타내었다. 불규칙하게 위치한 판상형의 EG가 압축 시 LCN2 사이에 일정하게 수평으로 위치한다. 따라서 100 MPa로 압축된 95 wt% LCN2 – 5 wt% EG 복합체의 반지름 방향 열전도도는 LCN2 성형체보다 3배 이상 증가하였으며 MH 분말보다 10배 이상 증가하였다.

SEM ion mapping of LCN2 and EG; (a) mixed LCN2 and EG powder, (b) carbon mapping of mixed LCN2 and EG powder, (c) vertical section of compressed EG additive composite, (d) carbon mapping of vertical section of compressed EG additive composite
3.2 수소화 전후 95 wt% LCN2 – 5 wt% EG 복합체의 열전달 특성
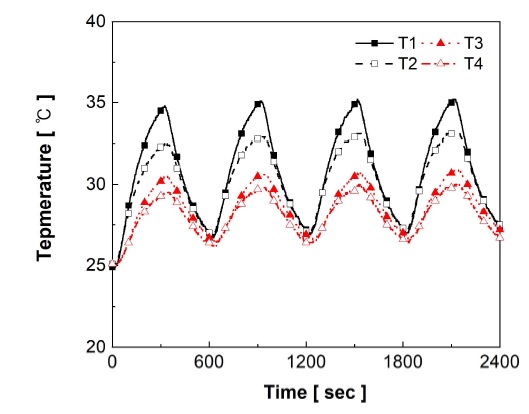
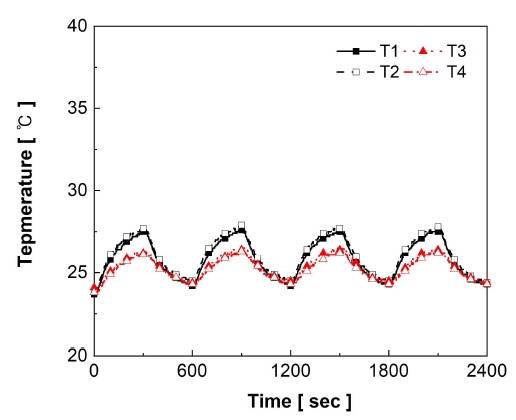
Fig. 5와 Fig. 6은 수소화 전후 95 wt% LCN2 – 5 wt% EG 복합체의 간헐적 열량 공급에 따른 온도 변화이다. 1, 2번 열전대에서 3, 4번 열전대로 온도의 최고점이 이동하는 데 소요된 시간은 수소화 전 약 11.3초, 수소화 후 약 7초이다. 수소화 전보다 수소화 후 열이 외부로 1.61배 빠르게 방출되었다. 열확산도는 수소화 전 약 4.98 mm2/s, 수소화 후에는 약 8.04 mm2/s로 산출되었다.
수소화 전 1, 2번 열전대의 최고 온도는 평균 34.0℃까지 상승하였으며 열이 전달된 3, 4번 열전대의 최고 온도는 평균 31.0℃로 측정되었다. 수소화 후 1, 2번 열전대의 최고온도는 평균 27.6℃이고 3, 4번 열전대의 최고온도는 평균 26.3℃이다.
복합체에서 사용한 LCN2와 동일한 La-Ni계 MH이면서 AB5계 MH를 대표하는 LaNi5를 대조시료로 선정하였다. 대조시료인 LaNi5의 열확산도는 약 1 mm2/s이다15). 95 wt% LCN2 - 5 wt% EG 복합체의 수소화 전과 수소화 후의 열확산도는 대조시료 LaNi5의 열확산도보다 각각 약 5배와 8배 높았다.
3.3 LCN2 분말과 95 wt% LCN2 – 5 wt% EG 복합체의 수소 저장 특성
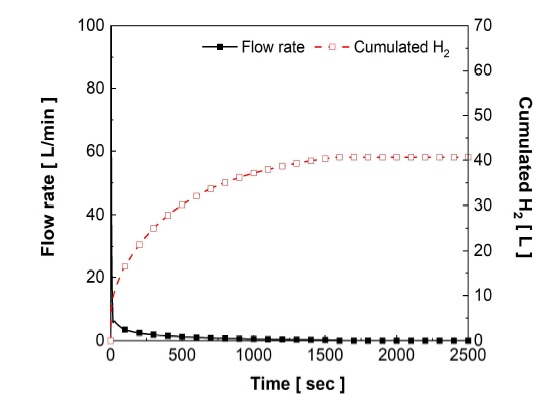
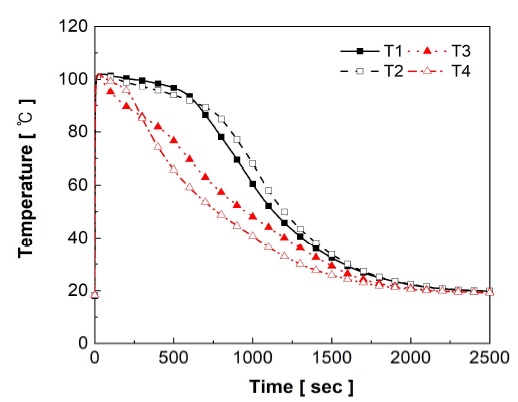
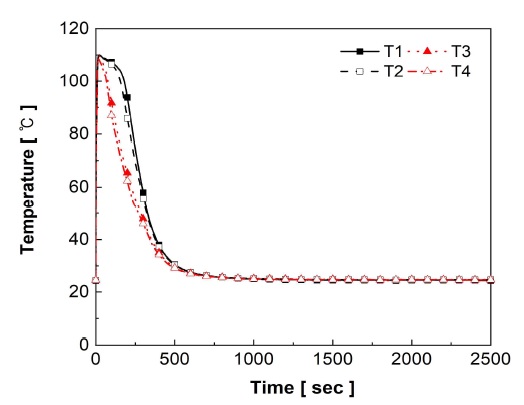
Fig. 7과 Fig. 8에 LCN2 분말과 95 wt% LCN2 – 5 wt% EG 복합체에 저장되는 수소의 유량 및 저장된 수소량을 각각 나타내었다. Fig. 9와 Fig. 10에 LCN2 분말과 95 wt% LCN2 – 5 wt% EG 복합체의 수소 저장 시 온도 변화를 나타내었다. LCN2 분말과 95 wt% LCN2 – 5 wt% EG 복합체는 각각 약 1,600초와 약 400초에 최대 저장량에 도달하였다. EG 5 wt% 혼합 및 압축성형은 수소 저장 시간을 1/4로 감소시켰다. LCN2 분말과 95 wt% LCN2 – 5 wt% EG 복합체 모두 각각의 수소 저장 시간과 유사한 시간 동안 최고 온도(100-110℃)를 유지하였다.
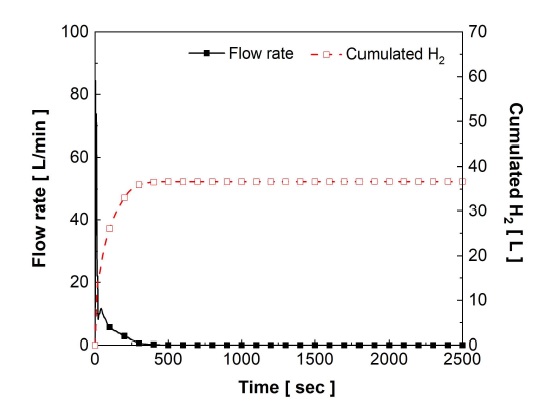
Flow rate and cumulated hydrogen inside the 95 wt% LCN2 – 5 wt% EG composite during hydrogen storage at 40 bar
LCN2 분말과 95 wt% LCN2 – 5 wt% EG 복합체 모두 수소 저장 초기에는 장치의 빈 공간을 채우기 위해 순간적으로 60 L/min 이상의 수소가 공급되었다. LCN2 분말은 20초 이후 수소 저장 유량이 10 L/min 이하로 내려갔으며 약 1,600초까지 수소가 저장되었다. 95 wt% LCN2 – 5 wt% EG 복합체는 약 50초까지 수소 저장 유량이 10 L/min으로 유지되었으며 이 후 서서히 감소하면서 400초까지 수소가 저장되었다. 반응 시작 후 LCN2 분말과 95 wt% LCN2 – 5 wt% EG 복합체는 각각 700초와 250초 동안 최고 온도를 유지하였다. 최고 온도가 유지되는 동안 수소 저장 유량이 일정하게 유지되었다. 이는 MH의 고유특성과 관련된다. 수소가 저장되는 압력을 나타내는 평탄압은 MH의 온도에 따라 달라진다. MH로의 수소 저장은 발열 반응이며, 발열 반응에 의한 MH의 온도 상승은 MH의 평탄압을 상승시킨다. 온도가 상승하여 평탄압이 수소 공급 압력과 같아지면 수소는 저장되지 않는다. 이때, 반응열을 제거하면 MH의 온도가 내려가고 평탄압이 감소하여 반응이 다시 진행된다. 즉, 반응열을 빨리 제거할수록 수소가 저장되지 않는 시간이 짧아진다. 이러한 이유로 LCN2 분말보다 열전도도가 높은 95 wt% LCN2 – 5 wt% EG 복합체가 LCN2 분말에 비해 4배 빠르게 수소를 저장하였다.
4. 결 론
본 연구에서는 EG 혼합 및 압축성형이 LCN2의 열전달 특성 및 수소 저장 특성에 미치는 영향을 확인하였으며, 다음과 같은 결론을 얻었다.
1) 100 MPa로 압축된 95 wt% LCN2 – 5 wt% EG 복합체의 반지름 방향 열전도도가 LCN2 분말보다 10배 이상, LCN2 성형체보다 3배 이상 증가하였다. 5 wt% EG 혼합 및 100 MPa 압축성형은 열전달 특성 향상에 효과적이다.
2) 95 wt% LCN2 – 5 wt% EG 복합체의 열전달 특성 평가에서 복합체의 열확산도는 대조시료 LaNi5의 열확산도와 비교하였을 때 수소화 전 약 5배, 수소화 후 약 8배 증가하였다. 복합체의 열확산도는 수소 가스의 존재 및 LCN2의 팽창에 의해 수소화 전보다 수소화 후에 1.61배 증가하였다.
3) LCN2 분말과 95 wt% LCN2 – 5 wt% EG 복합체 각각에 대한 수소 저장 특성 평가에서 최고 온도는 100-110℃로 비슷하였으나 95 wt% LCN2 – 5 wt% EG 복합체는 열전달 특성이 향상되어 LCN2 분말보다 수소를 4배 빠르게 저장하였다. EG 첨가는 반응열에 의해 높아진 MH의 온도를 효율적으로 낮추며 수소 저장 속도를 향상시킨다.
Acknowledgments
본 연구는 국토교통부/국토교통과학기술진흥원의 지원으로 수행되었습니다(과제번호 20HSCT-B157909-01).
References
-
B. Sakintuna, F. Lamari-Darkrim, and M. Hirscher, “Metal hydride materials for solid hydrogen storage: a review”, Int. J. Hydrogen Energy, Vol. 32, No. 9, 2007, pp. 1121-1140.
[https://doi.org/10.1016/j.ijhydene.2006.11.022]

-
O. Bernauer, “Metal hydride technology”, Int. J. Hydrogen Energy, Vol. 13, No. 3, 1988, pp. 181-190.
[https://doi.org/10.1016/0360-3199(88)90017-1]

-
C. S. Park, K. J. Jung, S. U. Jeong, K. S. Kang, Y. H. Lee, Y. S. Park, and B. H. Park, “Development of hydrogen storage reactor using composite of metal hydride materials with ENG”, Int. J. Hydrogen Energy, Vol. 45, No. 51, 2020, pp. 27434-27442.
[https://doi.org/10.1016/j.ijhydene.2020.07.062]

-
B. D. MacDonald and A. M. Rowe, “Impacts of external heat transfer enhancements on metal hydride storage tanks”, Int. J. Hydrogen Energy, Vol. 31, No. 12, 2006, pp. 1721-1731.
[https://doi.org/10.1016/j.ijhydene.2006.01.007]

-
P. Muthukumar, M. P. Maiya, and S. S. Murthy, “Experiments on a metal hydride-based hydrogen storage device”, Int. J. Hydrogen Energy, Vol. 30, No. 15, 2005, pp. 1569-1581.
[https://doi.org/10.1016/j.ijhydene.2004.12.007]

-
T. Oi, K. Maki, and Y. Sakaki, “Heat transfer characteristics of the metal hydride vessel based on the plate-fin type heat exchanger”, J. Power Sources, Vol. 125, No. 1, 2004, pp. 52-61.
[https://doi.org/10.1016/S0378-7753(03)00822-X]

-
G. Mohan, M. P. Maiya, and S. S. Murthy, “Performance simulation of metal hydride hydrogen storage device with embedded filters and heat exchanger tubes”, Int. J. Hydrogen Energy, Vol. 32, No. 18, 2007, pp. 4978-4987.
[https://doi.org/10.1016/j.ijhydene.2007.08.007]

-
A. Boukhari and R. Bessaïh, “Numerical heat and mass transfer investigation of hydrogen absorption in an annulus-disc reactor”, Int. J. Hydrogen Energy, Vol. 40, No. 39, 2015, pp. 13708-13717.
[https://doi.org/10.1016/j.ijhydene.2015.05.123]

-
M. Dieterich, C. Pohlmann, I. Bürger, M. Linder, and L. Röntzsch, “Long-term cycle stability of metal hydride-graphite composites”, Int. J. Hydrogen Energy, Vol. 40, No. 46, 2015, pp. 16375-16382.
[https://doi.org/10.1016/j.ijhydene.2015.09.013]

-
C. Pohlmann, L. Röntzsch, T. Weißgärber, and B. Kieback, “Heat and gas transport properties in pelletized hydride–graphite-composites for hydrogen storage applications”, Int. J. Hydrogen Energy, Vol. 38, No. 3, 2013, pp. 1685-1691.
[https://doi.org/10.1016/j.ijhydene.2012.09.159]

-
K. Herbrig, L. Röntzsch, C. Pohlmann, T. Weißgärber, and B. Kieback, “Hydrogen storage systems based on hydride–graphite composites: computer simulation and experimental validation”, Int. J. Hydrogen Energy, Vol. 38, No. 17, 2013, pp. 7026-7036.
[https://doi.org/10.1016/j.ijhydene.2013.03.104]

-
H. Imamura, S. Tabata, N. Shigetomi, Y. Takesue, and Y. Sakata, “Composites for hydrogen storage by mechanical grinding of graphite carbon and magnesium”, Int. J. Hydrogen Energy, Vol. 330-332, 2002, pp. 579-583.
[https://doi.org/10.1016/S0925-8388(01)01506-7]

- S. Y. Noh, Y. W. Rhee, K. S. Kang, S. J. Choi, and J. W. Kim, “Technology characteristics of hydrogen storage and its technology trend by the patent analysis”, Trans Korean Hydrogen New Energy Soc, Vol. 19, No. 1, 2008, pp. 90-102. Retrieved from https://www.koreascience.or.kr/article/JAKO200818259610128.page, .
-
J. S. Kim, W. B. Han, H. S. Cho, M. S. Jeong, S. U. Jeong, W. C. Cho, K. S. Kang, C. H. Kim, K. K. Bae, J. W. Kim, and C. S. Park, “Hydrogen storage and release properties for compacted Ti-Mn alloy”, Trans Korean Hydrogen New Energy Soc, Vol. 28, No. 1, 2017, pp. 9-16.
[https://doi.org/10.7316/KHNES.2017.28.1.9]

-
X. Lin, Q. Zhu, H. Leng, H. Yang, T. Lyu, and Q. Li, “Numerical analysis of the effects of particle radius and porosity on hydrogen absorption performances in metal hydride tank”, Applied Energy, Vol. 250, 2019, pp. 1065-1072.
[https://doi.org/10.1016/j.apenergy.2019.04.181]

-
A. N. Kazakov, I. A. Romanov, V. N. Kuleshov, and D. O. Dunikov, “Experimental investigations of adsorption characteristics and porosity of activated metal hydride powders”, Journal of Physics : Conference Series, Vol. 891, 2017, 012115.
[https://doi.org/10.1088/1742-6596/891/1/012115]

-
C. S. Park, J. W. Kim, K. K. Bae, S. U. Jeong, and K. S. Kang, “Investigation of thermal management parameters of metal hydride based hydrogen storage system”, Trans Korean Hydrogen New Energy Soc, Vol. 29, No. 3, 2017, pp. 251-259.
[https://doi.org/10.7316/KHNES.2018.29.3.251]