SOFC 스택 적용 마이크로웨이브-매트릭스 개질기 개발
2021 The Korean Hydrogen and New Energy Society. All rights reserved.
Abstract
In this study, a novel microwave-matrix reformer was proposed to convert CH4, which is a major component, to a high quality hydrogen energy. And to identify this performance, it was investigated for O2/C ratio, steam feed amount and reformed gas recirculation which are affected for methane conversion and product gas yield. Through the parametric screening studies, optimal operating conditions were that O2/C ratio, steam feed amount and recirculation rate were 1.1, 10 mL/min and 30 L/min. In this conditions, CH4 conversion was 68.1%, H2 selectivity 77.2 and H2/CO ratio 2.62 which are possible applying SOFC stack for RPG (residential power generator).
Keywords:
Partial oxidation reforming, Microwave heating, Matrix burner, Fuel cell, Hydrogen production키워드:
부분산화 개질, 마이크로웨이브 가열, 매트릭스 버너, 연료전지, 수소생산1. 서 론
메탄은 천연가스, 쉐일가스, 코크오븐가스, 바이오가스 등이 함유하고 있는 가스이다.
온실가스인 메탄을 양질의 연료로 전환하는 기술은 기존의 열적 전환과 그 외 대체 기술로 전기화학적 전환, 태양 열화학적 전환, 광-화학적 전환, 바이오-화학적 전환이 있다1-3).
열적전환 방법으로는 수증기개질법4,5), 건식개질6,7) 그리고 부분산화개질법8)이 있다. 수증기개질은 현재 실용화되어 산업분야에서 상용되고 있는 방법이지만 메탄 건식개질이 더 효과적인 방법으로 알려져 있다. 이는 건식개질이 온실가스인 이산화탄소 저감이 되고 효과적인 에너지 전환이 가능하기 때문이다. 부분산화개질은 수증기개질과 건식개질과 달리 발열 반응이므로 에너지 소모가 적은 특징을 가지고 있다9,10).
현재 산업분야에 적용되어 사용되고 있는 자열개질은 촉매 부분산화개질에 수증기개질 방식(또는 이산화탄소개질)이 결합된 형태이다. 이 경우 용량이 큰 산업분야에서 수소생산이 가능한 장점이 있으나 촉매사용에 의한 피독 문제, 수증기 생산 비용 증가 등의 문제가 있다. 이러한 문제를 해결하기 위해서는 새로운 진보된 기술개발이 필요하다.
본 연구에서는 새로운 타입의 마이크로웨이브 가열 축열식 매트릭스 개질기를 개발하고자 하였다. 축열식 매트릭스 버너 형태의 개질기는 개질기 챔버내 3차원적 체적을 가진 형태를 유지하고 그 내부로 조사되는 마이크로웨이브에 의해 수용체가 가열되어 안정되고 효율이 높은 부분산화개질이 이루어지는 방식이다. 매트릭스 버너의 표면 연소는 고온의 표면 다공성체에서 발생되는 복사열을 이용하여 유입되는 혼합가스가 가열되어 연소의 안정성을 높이는 연소기술이다. 다공체 매트릭스로 유입되는 예혼합기가 반응 영역대에서 연소되고, 다공체에 축적된 일부 연소열은 높은 엔탈피 분위기에서 지속적인 안정된 연소가 가능하게 된다11,12).
본 연구에서는 새로운 형태의 개질기를 제안하고 개질성능 특성을 파악하기 위해 메탄 공급 시 O2/C비, 스팀 공급량, 개질가스 재순환율에 대한 개질 전환 특성을 파악하였다. 또한, 이러한 변수별 개질 전환 성능을 근거로 하여 각 경우에 대한 최적 전환 운전 조건을 제시하였다.
2. 실험장치 및 방법
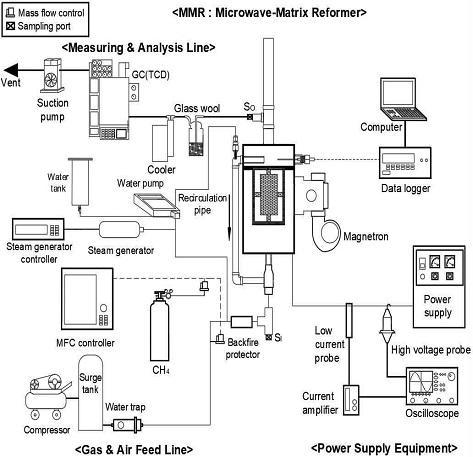
Fig. 1은 천연가스 주성분인 메탄을 연료로 SOFC 스택 적용가능한 수소를 생산하기 위한 마이크로웨이브-매트릭스 개질기(microwave-matrix reformer, MMR) 실험장치의 구성도이다. 실험장치 구성은 마이크로웨이브-매트릭스 개질기, 가스-공기 공급라인, 전원 공급 장치, 측정 및 분석라인으로 구성되었다.
마이크로웨이브-매트릭스 개질기는 직사각형의 챔버 내에 직사각형의 다공물질(SiC)인 매트릭스로 되어있고 그 중심에 마이크로웨이브 수용체인 탄화규소 다공체가 설치되어 있다. 마이크로웨이브가 조사되는 마크네트론은 수용체 중심면과 일치되도록 챔버면에 설치되었다.
전원 공급 장치는 전기를 공급하는 파워서플라이(Model LUP1200Q, Luxtem, Seoul, Korea)와 전기적 특성을 측정하는 전압 및 전류 프루브 등으로 구성되었다.
가스-공기 공급 라인에서 공급 가스는 메탄, 공기 및 스팀 각각 공급되어 벤츄리 믹서에서 혼합되어 MMR로 공급된다. 메탄은 메탄 봄베에서 일정 토출압력으로 공급되고, 스팀은 물펌프에서 공급된 물이 스팀 발생기에서 스팀으로 전환되어 200℃로 공급된다. 공기 공급은 압축기로 압축된 공기는 유체 맥동을 방지하고 균일한 압력을 유지하기 위해 서지탱그를 통과하여 수분을 응축 제거하기 위해 실리카겔로 충전된 워터트랩을 통과한 후 공급되었다. 연소용 공기와 처리가스의 유량은 mass flow controller (MFC)를 통해 조절되었다.
측정 및 분석라인은 MMR의 입구와 후단부에 샘플링 포트(Si, So)가 설치되어 있고 각각 전환된 생성가스를 포집한다. MMR에서 전환된 생성가스는 검뎅(soot)를 제거하기 위해 석면을 거친 후 냉각기(JEIO TECH HC-30, Jeio Tech, Inc., Billerica, MA, USA)을 거침으로 -20℃에서 가스를 냉각시켜 수분을 응축시키며 흡입펌프(LABOPORT® N 840.3 FT.18, KnF, Freiburg, Germany)에 의해 샘플링된다. 샘플링된 가스의 주요 가스인 CH4, CO2, H2, CO 등이 분석 장비인 GC-TCD (CP-4900, Varian Inc., Palo Alto, CA, USA)를 통해 분석된다. MMR 내의 가스 온도는 데이터로거(FLUKE 2625A HYDRA, Fluke Corporation, Tokyo, Japan) 및 열전대(K-type, 직경 0.3 mm)에 의해 측정되었다.
마이크로웨이브-매트릭스 개질기를 개발하고자 마이크로웨이브 가열 축열식 매트릭스 부분산화 연소기를 설계·제작하고 이에 대한 메탄의 개질특성에 영향을 미치는 요소에 대해 실험적 연구를 진행하였다. Table 1은 각 변수별 실험범위이고 기준 조건(reference condition)은 각 실험변수의 최적조건이다.
실험 방법은 개질연료인 메탄과 부분산화 산화제인 공기가 일정 공기비에 맞게 각각 MFC로 조절된 후 벤츄리 가스혼합기에서 혼합되어 MMR로 공급되었다. 개질가스 재순환 실험의 경우 재순환으로 공급되는 최대량에 실제 공급되는 양의 비를 코크 밸브로 조절하면 실험이 진행되었다. 스팀 공급량은 환산된 물의 양이 물펌프에서 조절된 후 스팀발생기에 스팀으로 전환되어 공급되었다. 마이크로웨이브 공급 전력은 1 kW로 일정하게 공급되었다.
생성가스 분석은 GC (CP-4900, Varian Inc.)가 이용되었으며, Molecular Sieve 5A capillary column (Model MS 5A, Varian Inc.)에서 H2, O2, N2, CH4, CO를 분석하고 PoraPLOT Q capillary column (Agilent, Santa Clara, CA, USA)으로 CO2, C2H4, C2H2, C2H6 및 C3H8을 분석하였다.
MMR의 성능을 표현하기 위해 CH4 전환으로 나타내었으며, 식 (1)과 같이 계산되었다13).
| (1) |
여기서, CE는 CH4 전환(%)이고, [PG]input는 주입된 CH4의 유량(L/min), [PG]output는 배출된 CH4의 유량(L/min)이다.
생성된 가스의 수소 선택도(H2 selectivity), H2/CO 비는 다음 식 (2)와 식 (3)을 통해 구해졌다.
| (2) |
| (3) |
3. 실험 결과 및 토의
본 연구에서 마이크로웨이브-매트릭스 개질기 개발을 위하여 O2/C비, 스팀 공급량, 재순환율 각각 메탄개질에 영향을 주는 영향인자에 대해 변수별 연구를 진행하였고, 그 결과는 다음과 같다.
3.1 O2/C비 영향
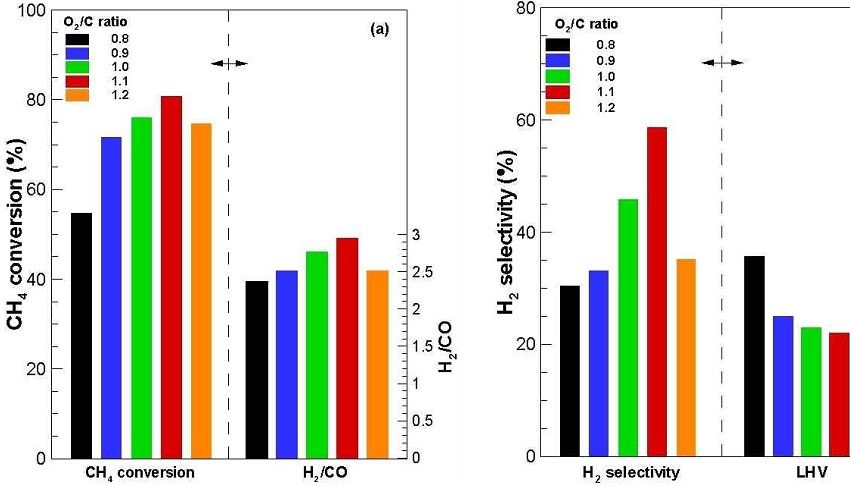
Fig. 2는 메탄만 공급되는 상태에서 전체 가스 공급량을 30 L/min으로 고정하고, O2/C비를 0.8-1.2까지 변화시켜 실험을 진행했을 때 개질특성을 나타낸 것이다. 이 경우 실험변수(Table 1 참조) 중 스팀공급과 재순환은 이루어지지 않은 상태이다. 이 때 매트릭스 개질버너 선단의 온도는 약 500℃로 유지되었다.
Fig. 2(a)에서 보이는 바와 같이 O2/C가 증가될수록 CH4 전환이 증가되어 O2/C비가 1.1일 때 최댓값 80.7%를 가진 후 다시 감소되었다. 공기의 공급량이 증가됨에 따라 CH4 전환이 증가되는 것은 메탄 부분산화반응 식 (4)가 활성화되어 메탄이 감소되고 H2와 CO가 증가되었기 때문이다.
그러나 CH4 전환이 최댓값을 가진 후 감소되는 데, 이는 환원성 분위기에서 부분산화반응에 의해 다량 생성된 H2와 CO가 건조개질의 역반응 식 (5)에 의해 CH4의 양이 다소 증가되었기 때문이다.
| (4) |
| (5) |
H2/CO비 역시 CH4 전환과 유사한 패턴을 보였으며 O2/C비 1.1에서 최댓값 2.95를 가졌다. 최댓값을 보인 후 H2/CO비가 감소되는 것은 산소의 양이 증가됨에 따라 다음 산화반응 식 (6)에 의해 H2의 양이 감소되었기 때문이다.
| (6) |
Fig. 2(b)는 개질 생성가스의 H2 선택도(H2 selectivity)와 저위발열량(Lower Heating Value, LHV)을 나타낸 것이다. H2 선택도는 H2/CO비의 패턴에서 예견하였듯이 유사한 패턴을 보였으며 O2/C비가 1.1에서 58.6으로 최댓값을 보였다. 저위발열량은 O2/C비 값이 작을수록 큰 값을 보였는데 이는 공급연료인 CH4가 전환되지 못한 상태로 생성가스에 그대로 존재하였고 전환된 가연성분인 CO, H2, CH4, THCs (C2H2, C2H4, C2H6)의 양도 작았기 때문이다.
Table 2는 생성가스 농도와 저위발열량을 나타낸 것이다. 생성가스는 O2/C비가 증가되어 1.1까지 공급연료인 CH4는 전환되어 감소되었고 그 외 가스인 CO2, CO, H2, THCs는 증가되었다. 그러나 O2/C비가 1.2에서는 상대적으로 산화성 조건이 되어 이미 생성된 H2는 식 (6)에 의해 H2O로 CO는 CO2로 일부 전환되어 그 값이 다소 증가되었다. 그리고 O2/C가 증가됨에 따라 전체 가연분이 포함된 LHV1은 감소되었고, H2와 CO만 고려된 LHV2는 O2/C가 1.1일 때 최댓값 246.98 MJ을 가진 후 감소되었다. LHV1의 감소는 O2/C비가 증가에 따라 CH4 공급량이 감소되어 잔류량이 감소되었기 때문이고, LHV2는 CH4가 H2와 CO로 전환된 양이 최대인 O2/C비가 1.1일 때 최대를 보였다.
3.2 스팀공급의 영향
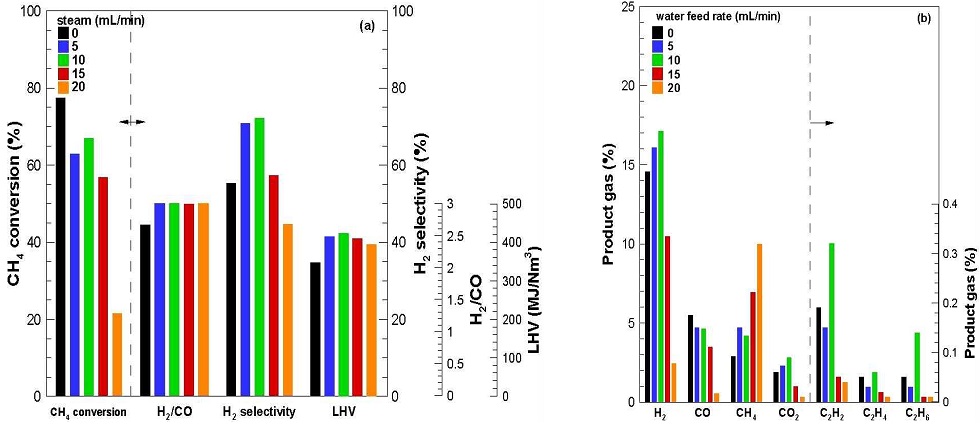
Fig. 3은 스팀발생기에서 생성된 스팀이 유입되는 메탄과 공기와 함께 벤츄리믹서에서 혼합되어 마이크로웨이브-매트릭스 개질기로 유입되는 경우이다. 이 때 스팀공급량은 5, 10, 15, 20 mL/min로 각각 공급되었고 그 외는 Table 1의 기준조건에서 진행되었다.
Fig. 3(a)는 CH4 전환율, H2/CO비, H2 선택도 그리고 저위발열량을 나타낸 것이다.
CH4 전환율은 스팀의 공급량이 증가되어 최댓값 67%를 보인 후 감소되었다. 스팀공급량이 증가됨에 따라 CH4 전환이 증가되는 것은 스팀 개질반응 식 (7)이 증가되었기 때문이다. 그러나 CH4 전환이 최댓값을 가진 후 감소되는데, 이는 환원성 분위기에서 스팀 개질반응에 의해 다량 생성된 H2와 CO가 건조개질의 역반응 식 (5)에 의해 CH4과 CO2로 전환되었기 때문이다.
그러나 스팀이 공급될 경우 스팀 공급이 안될 경우 보다는 CH4 전환율이 작은 값을 보였는데 이는 부분산화개질반응(식 [4]) 그리고 CO2 개질의 역반응 식 (5)이 상대적으로 약해지기 때문이다. 스팀이 공급될 경우가 공급되지 않은 경우보다 H2/CO비가 큰 값을 보이나 그 양이 증가될수록 감소되었다. 이는 수증기가 공급됨에 따라 다음 반응(식 [7], [8])이 진행되어 H2와 CO가 증가되지만 이미 생성되어진 H2가 산화반응(식 [6])에 의해 진행되어 H2/CO비가 감소되는 것을 알 수 있다. 개질 생성가스의 H2 선택도와 발열량은 스팀 공급량이 10 mL/min일 때 각각 72.2와 423.73 MJ/Nm3로 최댓값을 보였다.
| (7) |
| (8) |
Fig. 3(b) 개질가스의 농도를 나타낸 것이다. CH4 전환율이 최대인 스팀공급량이 10 mL/min일 때 H2와 CO2가 최댓값을 보였고 CH4은 최솟값을 나타내었다. 이는 이미 언급된 스팀 개질반응 식 (7)이 우수하였기 때문이다. 이 조 건의 경우 H2 선택도와 발열량도 최댓값을 가지므로 스팀이 주입구로 공급될 경우 최적 운전조건임을 알 수 있다.
3.3 생성가스 재순환의 영향
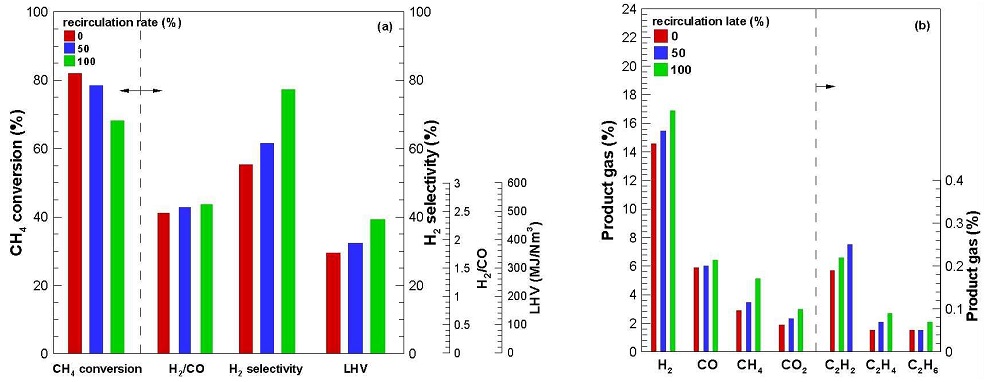
Fig. 4는 메탄개질의 기준조건인 전체 가스 공급량을 30 L/min, O2/C비를 1.1로 고정한 상태에서 개질가스의 일부를 재순환할 경우 개질 특성을 나타낸 것이다.
Fig. 4(a)는 CH4 전환율을 나타낸 것으로 재순환을 하지 않았을 때는 82.1%이고, 재순환율을 50%, 100%로 변화하였을 때 각각 78.4%, 68.1%로 상대적으로 작은 값을 보였다. 이는 CH4 전환이 감소되였다기보다는 재순환가스 중 포함된 미전환된 CH4으로 인해 개질기 내 농도가 증가되어 출구에서 그 농도에서 더 측정되기 때문이다.
그리고 H2/CO비와 H2 선택도도 재순환이 진행되지 않았을 때 2.47, 55.3%에서 재순환이 진행됨에 따라 점차 증가되어 재순환율이 100%일 때 그 값이 각각 2.62, 77.2%로 증가되었다. 이는 Fig. 4(b)의 생성가스 농도의 H2와 CO의 농도에서 확인되듯이 재순환 되지 않을 때 각각의 농도가 14.6%, 5.9%인데 재순환율이 증가됨에 따라 그 값이 증가되고 재순환율이 100%일 때 그 값이 각각 16.9%와 6.4%로 증가되었기 때문이다.
이상에서 알 수 있는 바와 같이 개질가스 재순환 시 가연가스인 H2와 CO 생성량이 증가되었으며, H2/CO비 특히 수소 선택도가 상대적인 수소증가로 인해 개선되었음은 물론이고 이 때 발열량이 높아 양질의 고품위 가스 생산이 가능한 것을 알 수 있다.
Table 3은 이상의 변수별 연구를 통해 MMR의 메탄 부분산화개질의 최적의 운전 조건과 결과이다. O2/C비가 1.1이고 전체 가스 공급량이 30 L/min일 때 CH4 전환은 68.1%이고, H2 선택도는 77.2%이고, H2/CO비는 2.62였다.
현재 상용화되어 사용되고 있는 촉매 자열개질 방식은 촉매 활성온도 유지를 위한 경제성 문제 그리고 촉매 비용과 내구성 문제가 있다. 본 연구 결과는 주거용열병합시스템(residential power generator, RPG)용 연료전지인 고체산화물형 연료전지(solid oxide fuel cell, SOFC) 스택(stack)에 적용하여 상기에 언급된 문제를 해결 가능할 것으로 판단된다.
4. 결 론
본 연구에서는 새로운 형태의 마이크로웨이브-매트릭스 개질기를 제안하고 메탄 공급 시 O2/C, 스팀공급량, 개질가스 재순환에 대한 개질 전환 특성을 파악하였다. 또한, 이러한 변수별 개질 전환 성능을 근거로 하여 각 경우에 대한 최적 전환 운전조건을 제시하였다.
첫째, CH4 전환, H2 선택도는 O2/C비가 증가됨에 따라 증가되어 1.1에서 최댓값을 가진 후 감소되었다. 그러나 저위발열량(LHV)은 O2/C비가 증가될 수록 감소되었다 둘째, 스팀이 주입구로 공급될 경우 그 공급량이 10 mL/min일 때 CH4 전환과 개질가스의 주요가스인 H2와 H2 선택도 그리고 발열량도 최댓값을 가지는 최적조건이 존재하였다. 셋째, 개질가스 재순환 시 H2와 CO 생성량이 증가되었으며, 특히 수소증가가 상대적으로 크기 때문에 수소선택도와 H2/CO비가 개선되었음은 물론이고 이 때 발열량이 높아 양질의 고품위 가스 생산이 가능한 것을 알 수 있다.
변수별 연구를 통해 MMR의 메탄의 부분산화개질 최적운전 조건이 존재하는 것을 확인하였으며 그 조건과 주요 성능 값은 O2/C비가 1.1이고 전체 가스 공급량이 30 L/min일 때 메탄전환은 68.1%이고 H2 선택도는 77.2%이고 H2/CO비는 2.62였다. 이상의 결과는 주거용열병합시스템용 연료전지인 고체산화물형 연료전지에 적용 가능할 것으로 판단된다.
Acknowledgments
이 논문은 2021학년도 조선대학교 학술연구비 지원을 받아 연구되었습니다.
References
-
R. Snoeckx and A. Bogaerts, “Plasma technology-a novel solution for CO2conversion”, Chem. Soc. Rev., Vol. 46, No. 19, 2017, pp. 5805-5863.
[https://doi.org/10.1039/C6CS00066E]

-
H. S. Song, S. J. Kwon, W. Epling, and E. Crosiet, “Synthesis gas production via partial oxidation, CO2 reforming, and oxidative CO2 reforming of CH4 over a Ni/Mg-Ai hydrotalcite-type catalyst”, Clean Technology, Vol. 20, No. 2, 2014, pp. 189-201.
[https://doi.org/10.7464/ksct.2014.20.2.189]

-
J. H. Hong, H. J. Ha, and J. D. Han, “The promotion effects on partial oxidation for methane for hydrogen production over Co/Al2O3 and Ni/Al2O3 catalsts”, Clean Technology, Vol. 18, No. 1, 2012, pp. 95-101.
[https://doi.org/10.7464/ksct.2012.18.1.095]

-
P. Beckhaus, A. Heinzel, J. Mathiak, and J. Roes, “Dynamic of H2 production by steamreforming”, J. Power Sources, Vol. 127, No. 1-2, 2004, pp. 294-299.
[https://doi.org/10.1016/j.jpowsour.2003.09.026]

- U. R. Cheon, K. S. Ahn, and H. K. Shin, “Study on the characteristics of methanol steam reformer using latent heat of steam”, Trans Korean Hydrogen New Energy Soc, Vol. 29, No. 1, 2018, pp. 19-24.
-
S. G. Wang, Y. W. Li, J. X Lu, M. Y. He, and H. Jiao, “A detailed mechanism of thermal CO2 reforming of CH4”, J. Molecular. Structure, Vol. 673, No. 1-3, 2004, pp. 181-189.
[https://doi.org/10.1016/j.theochem.2003.12.013]

- D. B. Han and Y. S. Baek, “A simulation study on the synthesis of syngas from the reforming reaction of biogas”, Trans Korean Hydrogen New Energy Soc, Vol. 29, No. 1, 2018, pp. 1-10.
-
A.E. Lutz, R.W. Bradshaw, L. Bromerg, and A. Rabinovich, “Thermodynamic analysis of hydrogen production by partial oxidation reforming”, Int. J. Hydrogen Energy, Vol. 29, No. 8, 2004, pp. 809-816.
[https://doi.org/10.1016/j.ijhydene.2003.09.015]

-
L. Xu, Y. N. Liu, Y. J. Li, Z. Lin, X. X. Ma, and Y. L. Zhang, “Catalytic CH4 reforming with CO2 over activated carbon based catalysts”, Appl Catal A Gen, Vol. 469, 2014, pp. 387-397.
[https://doi.org/10.1016/j.apcata.2013.10.022]

-
L. Li, H. G. Wang, X. Jiang, Z. Song, X. Zhao, and C. Y. Ma, “Microwave-enhanced methane combined reforming by CO2 and H2O into syngas production on biomass-derived char”, Fuel, Vol. 185, 2016, pp. 692-700.
[https://doi.org/10.1016/j.fuel.2016.07.098]

-
T. Takeno and K. Sato, “An excess enthalpy flame theory”, Combustion Sience and Technology, Vol. 20, No. 1-2, 1979, pp. 73-84.
[https://doi.org/10.1080/00102207908946898]

-
A. I. Bakry, “Stabilized premixed combustion within atmospheric gas porous inert medium (PIM) burner”, Proceedings of the Institution of Mechanical Engineers. Part A, Journal of Power and Energy, Vol. 222, No. 8, 2008, pp. 781-789.
[https://doi.org/10.1243/09576509JPE608]

-
X. Tu and J. C. Whitehead, “Plasma dry reforming of methane in an atmospheric pressure AC gliding arc discharge: Co-generation of syngas and carbon nanomaterials”, Int. J. Hydrog. Energy, Vol. 39, No. 18, pp. 9658-9669.
[https://doi.org/10.1016/j.ijhydene.2014.04.073]